


2025年2月25日,Alnylam 召开了2025研发日活动(R&D Day),介绍了包括 INHBE siRNA 在内的 26 款产品的最新研究进展
2025年2月25日,Arrowhead 公布了 ARO-ALK7 的临床前结果
Who is the Best Healthy Weightloss Star?
鼎泰团队将在本文进行全景解读
全文共:5433 字 31 图
预计阅读时长:20 分钟
INHBE 与 ALK7,
生物学之外的 Interaction 时刻
在生物信息学数据的积累如涓涓细流汇成江海,转化研究证据日臻完善之际,以 siRNA 为技术底座、靶向调节关键基因的创新疗法正展现出突破代谢性疾病治疗瓶颈的无限潜能。其中,针对 ALK7 与 INHBE 这两个关键靶点的 siRNA 药物正被视为实现"减脂保肌"、“健康减重”目标的重要突破口。
前期,鼎泰团队已对 INHBE 和 ALK7 的信号通路、生物学功能和相关 siRNA 的初步非临床研究结果及其临床规划进行了深入解读。详见往期推文:
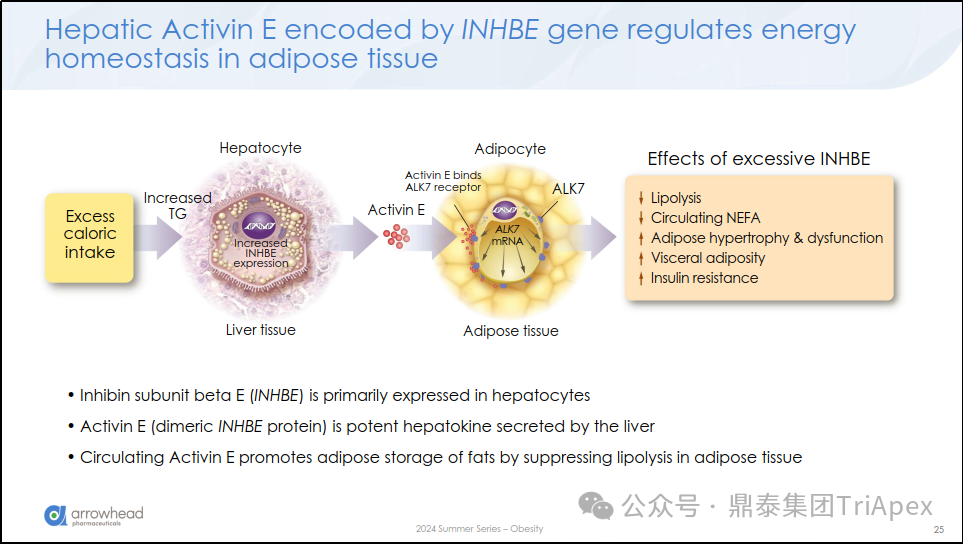
图1. INHBE 基因编码的 INHBE 调节脂肪组织能量平衡(资料来源:2024 Summer Series of R&D Webinars Part IV – Obesity Programs)
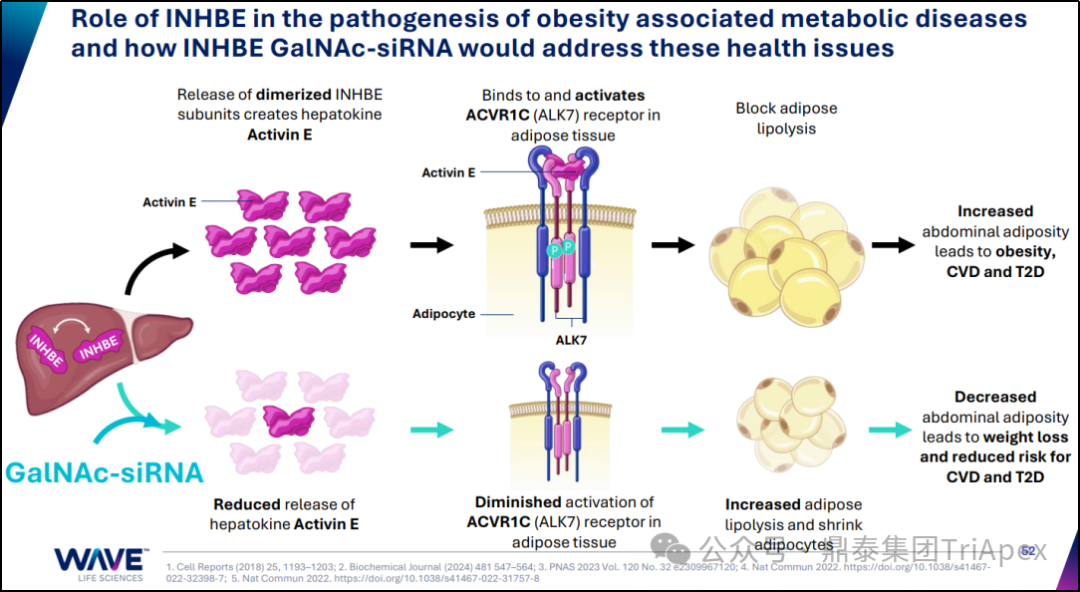
图2. INHBE 在肥胖相关代谢疾病发病机制中的作用及应用(资料来源:Research Day Wave Life Sciences October 30, 2024)
美好的事物,如同与高山与流水相映,往往在某时默契相遇;重大的科学突破,恰如繁星闪耀夜空,常常在某刻同辉。Alnylam 与 Arrowhead 两家 siRNA 药物研发企业的创新成果恰似双子星交汇,在同一片夜空为肥胖症靶向治疗领域注入了前所未有的活力与希望。
☆ Alnylam 在 2025 研发日活动上公布了其 INHBE siRNA 取得的重要进展,目前该产品已进入 IND 申请的关键准备阶段

☆ Arrowhead 同一天更新了 ALK7 siRNA 治疗肥胖症的临床前研究成果

尽管两家公司在研究策略、信息完整度、技术路线、研究数据等方面各有侧重,但均为国内相关领域的研发提供了极具价值的参考与启发。为响应两会“体重管理”的号召,本文将继续专注于 INHBE 和 ALK7 siRNA 这两个前沿方向,深入剖析最新研究成果,洞见潜力靶点的研究现状与未来趋势。
健康减重,
未满足的临床需求与破局之策
☆ 代谢性疾病的全球困局
全球范围内,代谢性疾病(包括肥胖症、II型糖尿病、代谢相关脂肪性肝炎等)有超 17 亿患者群体。司美格鲁肽和替尔泊肽 等 GLP-1 受体激动剂通过机制创新、给药途径改良和不断提高的临床获益改变了代谢性疾病治疗的格局。随之而来的,潜在的肌肉流失等副作用也引发了广泛关注。因此,健康的体重管理治疗方案可能是将来代谢性疾病治疗的新范式。
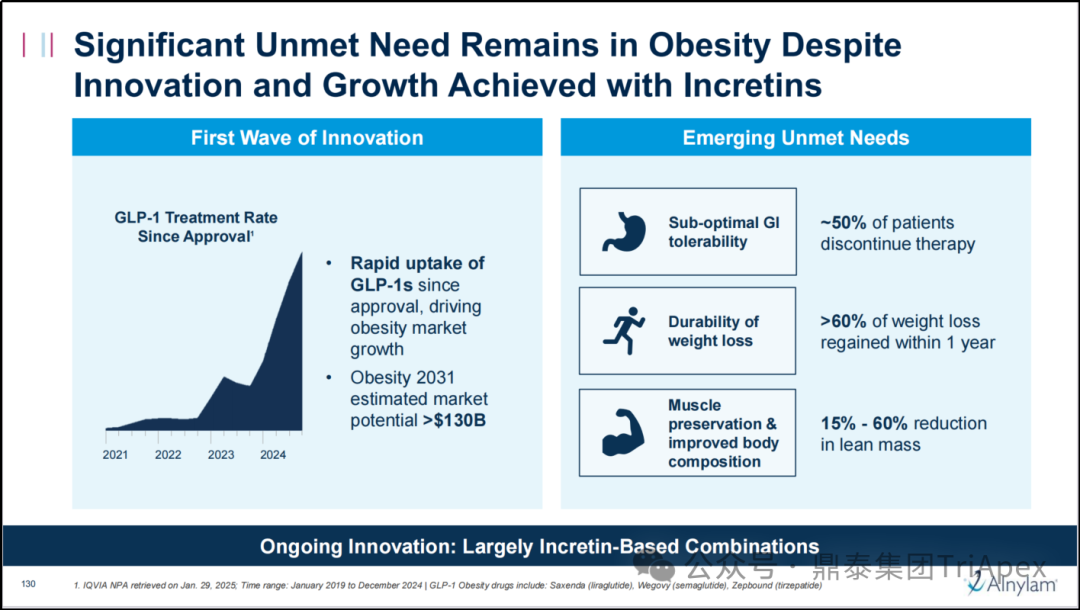
图3.肥胖症治疗存在未满足的临床需求(资料来源:Alnylam R&D DAY 2025)
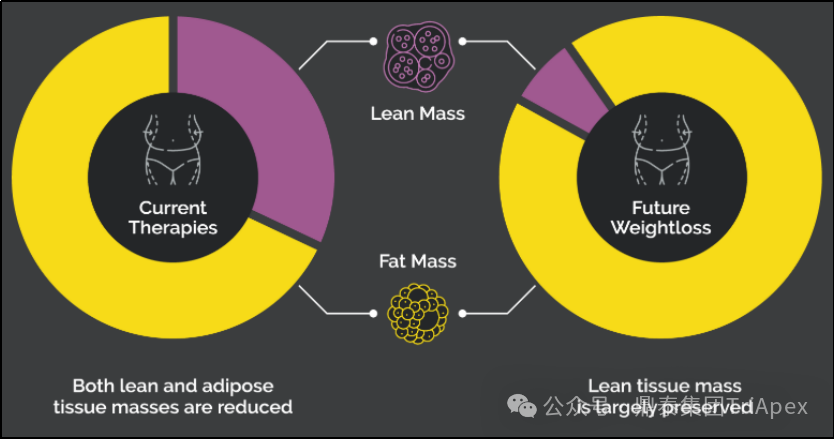
图4.健康体重管理的新范式(资料来源:网页资料)
☆ 破局之策
在本次研发日活动中,Alnylam 重点发布了其在代谢性疾病领域的全新战略蓝图,覆盖了肥胖症、II型糖尿病、NAFLD、高血压等重大疾病。该研究结果预示着 siRNA 研发企业正通过“基因沉默”技术挑战传统药物的边界,并用长效、靶向、组合疗法开启代谢性疾病治疗的新时代。
第一步:靶点的精准筛选
Alnylam 在代谢性疾病领域的发展基于扎实的人类遗传学研究。通过对与代谢性疾病密切相关的基因进行系统性筛选,锁定了包括 INHBE、ACVR1C、GPR75 和 GRB14等在内的多个潜力靶点。这些基因不仅在疾病病理过程中发挥重要作用,还在临床前概念验证试验中展现出充满期待的治疗潜力。
当然,Arrowhead 在这一方面的基础研究和转化效率也毫不逊色(本文暂不进行延伸),详见后文“临床试验前瞻”部分。
第二步:技术优势突破 siRNA 递送瓶颈
Alnylam 和 Arrowhead 均根据靶点特征开发了通过精准靶向肝脏和脂肪等关键组织的 siRNA 递送技术,有望实现每半年皮下注射给药 1 次的长间隔给药,从而显著提升了患者的治疗体验与依从性。相信关于两家公司产品布局、递送策略的更多信息和数据将陆续浮出水面。
第三步:联合用药释放协同效应
基于非临床概念验证数据的支持,两家公司正在探索将 siRNA 与现有标准治疗方案(如 GLP-1R 激动剂)联用的可能性。Alnylam 在本次研发日中还提及了与新机制 siRNA 联用的开发计划。这种“强强联合”策略不仅有望获得持续的体重降低(Durable weight loss),还能提高减重质量(Quality of weight loss)、提高耐受性(Improve tolerability)和减少停药率(Reduce discontinuation rate),从而覆盖更广泛患者群体的多样化需求。
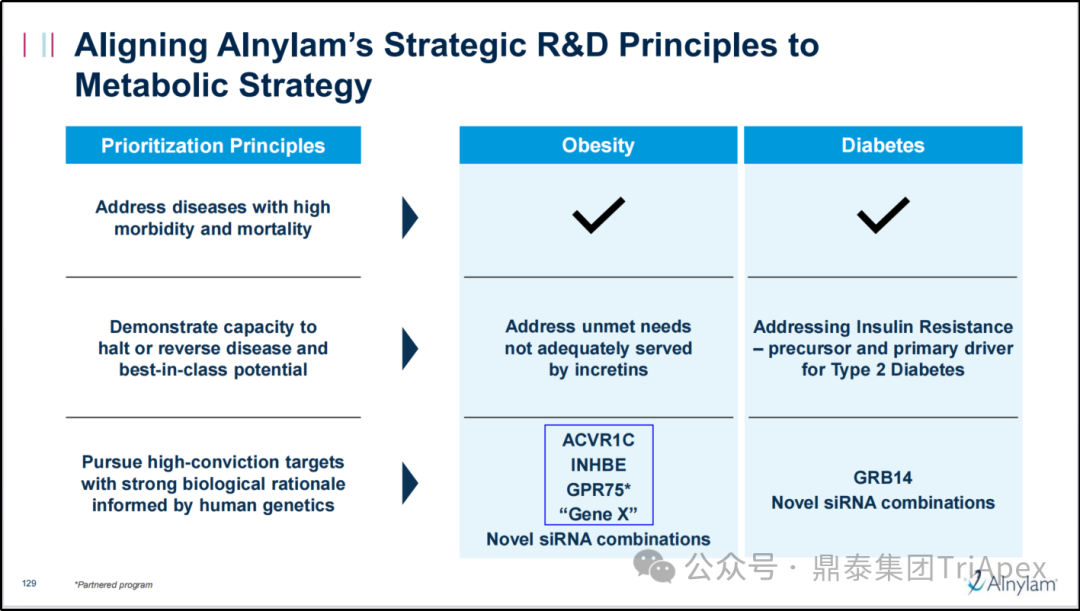
图5. Alnylam 在肥胖和糖尿病领域的战略布局(资料来源:Alnylam R&D DAY 2025)

图6.通过靶向 Inhibin/Activin 通路实现更安全和更持久的减重效果(资料来源:Alnylam R&D DAY 2025)
把肌留住,INHBE siRNA
非临床研究结果和临床试验进展更新
☆ 流水不争先
Alnylam 早在 2022 年 7 月率先发表文章揭示了 INHBE pLOF(预测的功能丧失)与较低的 WHRadjBMI(BMI调整后腰臀比)的相关性,并在 2023 年 12 月的研发日活动中披露了 ALN-INHBE 的初步临床前数据。
但客观地讲,从目前披露的数据和 ClinicalTrial.gov 临床试验登记情况来看,Alnylam 在 INHBE 上的进度暂时落后了!反倒是 Arrowhead 和 后来的 Wave Life Sciences 先后登记了I期临床试验的信息(详见后文)。
当然,我们深信新药研发是一个漫长且充满不确定性的历程,从来不是一城一池的得失可以决定结局的竞速,再加上 Alnylam 在 siRNA 领域数个成功商业化产品的娴熟经验(详见往期“他山之石”系列文章),将来胜出的概率仍然非常大。
☆ INHBE siRNA 数据更新
关于 ALN-INHBE,Alnylam 在本次研发日中更新的的资料不多,主要为 ALN-INHBE 在食蟹猴肝脏中可下调 INHBE 的表达以及在啮齿类动物模型中与司美格鲁肽联用时的减脂保肌数据,更详细的内容见往期推文《减脂保肌,INHBE 有态度,KBI 有招数》。
同时,为了更清晰地了解相关试验细节,鼎泰团队将该结果做成表格。
表1.Alnylam ALN-INHBE 非临床数据更新

除了上述纵向对比,鼎泰团队也同步汇总了 Arrowhead 和 WAVE 两家公司的研究数据。
表2.Arrowhead 和 WAVE INHBE siRNA 非临床数据对比
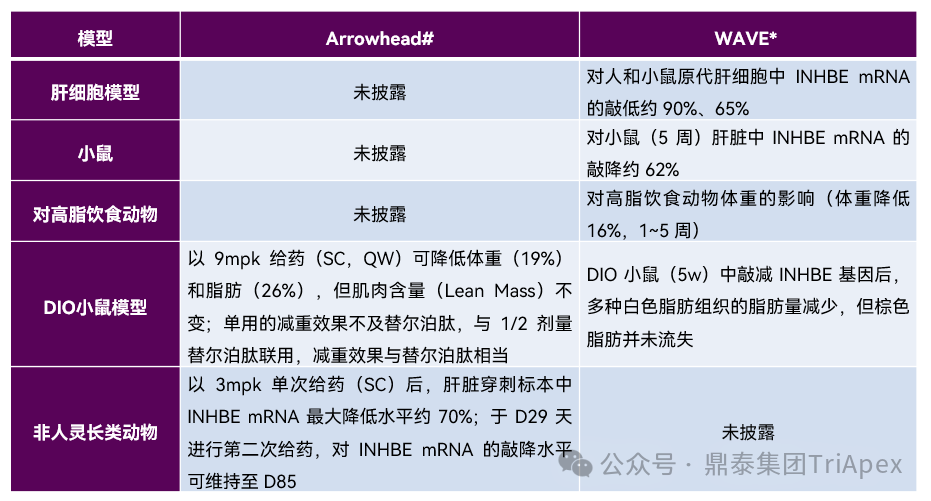
数据来源:#,2024 Summer Series of R&D Webinars Part IV – Obesity Programs(August 14, 2024)
*,Wave Life Sciences R&D Day(September 28, 2023)
此外,Alnylam 也在积极布局组合疗法,将上述长效 siRNA 疗法与低剂量司美格鲁肽联用,有望在提高减脂效果的同时,保持瘦体重质量并减少停用司美格鲁肽之后的体重反弹。

图7.长效 siRNA 与低剂量司美格鲁肽联用的效果(资料来源:Alnylam R&D DAY 2025)
值得特别关注的是,在 Alnymam(上)和 Arrowhead(下)公司公开的研究资料中,反复出现的这张关于 INHBE 蛋白检测的结果始终令人垂涎其背后的检测方法。我们不禁要问:
 究竟采用了何种具体方法学来测定这一指标?
究竟采用了何种具体方法学来测定这一指标?
 为何在研究设计中选择半定量评价手段而非更精准的检测方式?
为何在研究设计中选择半定量评价手段而非更精准的检测方式?
 在未来的临床试验策略中,是否将血浆中的 INHBE 水平作为疗效预测性生物标志物(biomarker)进行应用……
在未来的临床试验策略中,是否将血浆中的 INHBE 水平作为疗效预测性生物标志物(biomarker)进行应用……
这些问题目前尚不足以解答,仍然带有一定的神秘色彩。期待与业界同仁开展更深入的研究与探讨,共同推动早期概念验证谜底的揭晓。
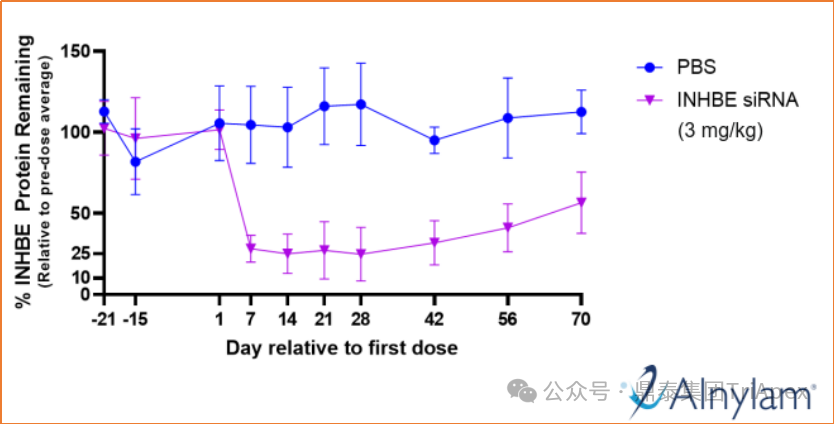
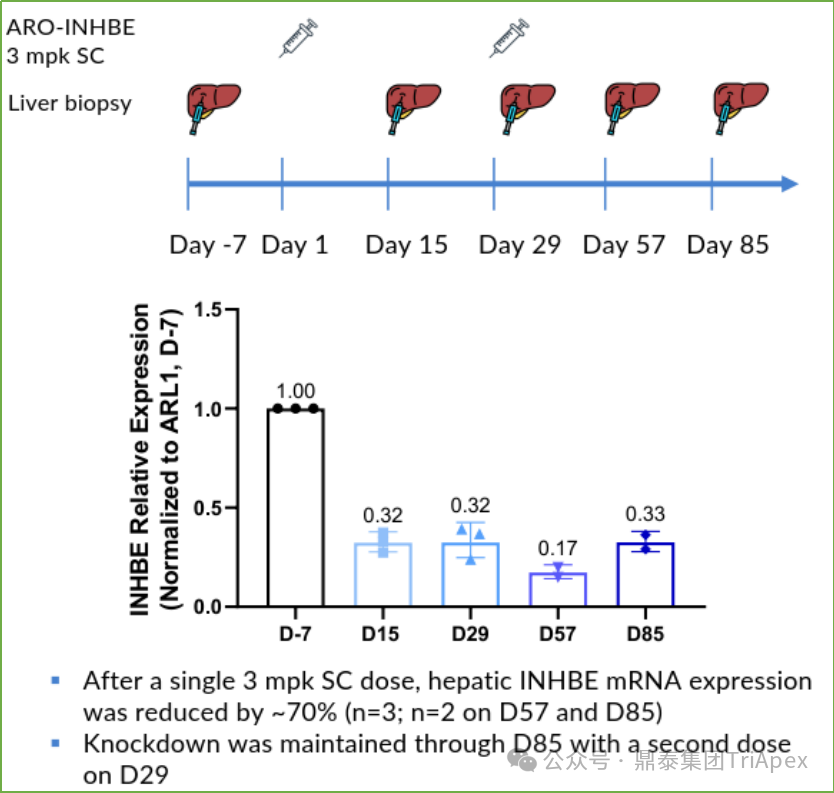
图8. INHBE 蛋白检测方法是什么?(资料来源:Alnylam和Arrowhead公开资料)
☆ 临床试验前瞻
(1)ALN-INHBE
如前文所述,截至研发日当天,尚未检索到 Alnylam 对于 ALN-INHBE 临床试验的登记情况。Alnylam 在 siRNA 领域的深厚积累,目前已有 5 款已上市药物,并有多个产品正在进行关键性临床试验或适应症拓展,能否通过更独到和娴熟的临床试验策略的复用实现反超值得期待。
推荐阅读
他山之石 | 已上市 siRNA 药物的临床开发路径和上市历程
(2)ARO-INHBE
Arrowhead 最早于 2024 年 9 月在新西兰获得 IND 批准,并在 12 月正式启动临床试验(NCT06700538),是当前针对 INHBE 进展最快的管线之一。
鼎泰团队根据 ClinicalTrial.gov 登记的信息,对其临床试验设计进行了分析。
⏩ 本研究为I/IIa期双盲剂量递增试验
单次及多次给予 ARO-INHBE 在肥胖成年受试者中的安全性、耐受性、药代动力学(PK)及药效动力学(PD)
在正接受替尔泊肽治疗的肥胖成年受试者中(伴或不伴II型糖尿病),重复给予 ARO-INHBE 的安全性、耐受性及 PD
第二部分将在完成第一部分多剂量组第 43 天的安全性数据评估后启动,其剂量选择将基于第一部分数据的综合分析。
⏩ 纳入标准
肥胖定义:在筛选时,BMI 在 30 至 50 kg/m²之间。既往减肥尝试 :至少有一次自我报告的、通过生活方式改变进行减肥但未成功的经历
依从性要求:愿意、能够且有动机遵守所有研究评估,并遵循研究方案的时间表,包括在整个研究期间坚持稳定的饮食和锻炼习惯
健康状况:在筛选时,没有临床相关的异常发现,这些异常可能会影响受试者安全或对研究结果产生不利影响(由研究者判断)
避孕措施
⏩ 试验设计
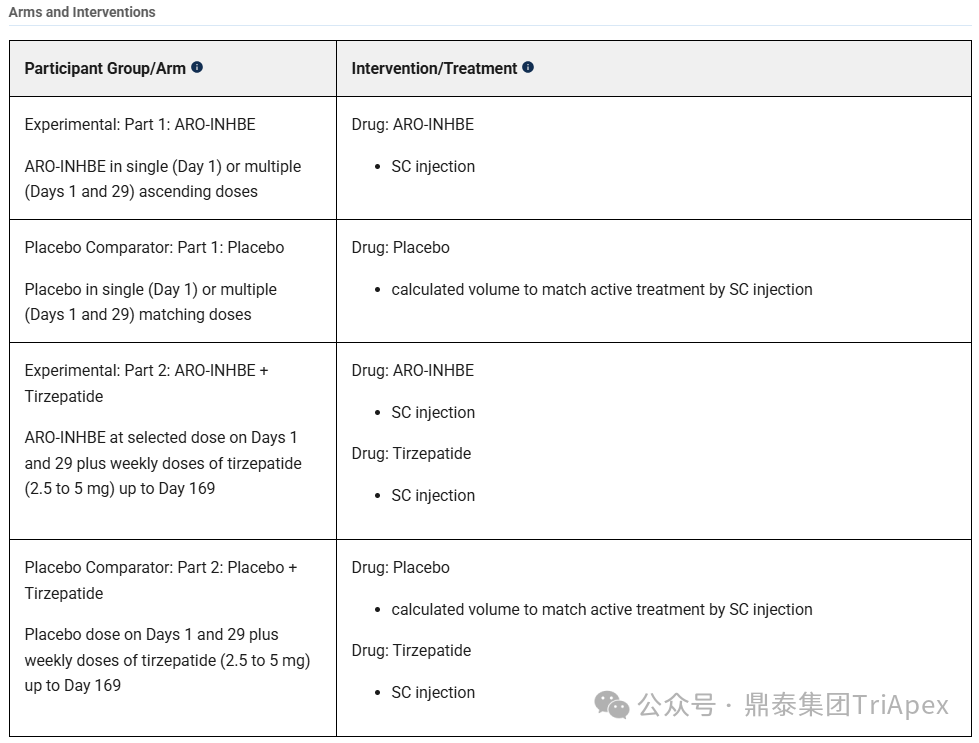
第 1 部分:ARO-INHBE
单次(第1天)或多次(第1天和第29天)递增剂量的 ARO-INHBE
单次(第1天)或多次(第1天和第29天)匹配剂量的安慰剂
第 2 部分:ARO-INHBE + 替尔泊肽
第1天和第29天选定剂量的 ARO-INHBE 联用每周剂量的替尔泊肽(2.5 至 5 mg),直至第169天
第1天和第29天的安慰剂剂量联用每周剂量的 替尔泊肽(2.5 至 5 mg),直至第169天
⏩ 主要终点
发生治疗中出现的不良事件 (TEAE) 的参与者人数
⏩ 次要终点
PK参数:Cmax、Tmax、AUC0-24、AUC0-t、AUC0-∞、T1/2、CL/F、Vz/F、Ae、Fe 、CLr
(3)WVE-007
WAVE 随后于 2025年2月25日(巧合还是预期的意外?)在 ClinicalTrial.gov 上登记了其临床试验的信息(NCT06842186)。从试验设计来看,笔者的体会是,WAVE 的设计谨慎了很多,亦或是缺少经验使然。

图9. NCT06842186 临床试验地点(资料来源:ClinicalTrials)
⏩ 试验目的
评估 WVE-007 在超重或肥胖成年患者中单次剂量递增 SC 给药后的安全性、耐受性、PK 和 PD
⏩ 试验设计
随机、双盲、安慰剂对照研究,共5个队列
⏩ 纳入标准
18 至 60岁的男性及女性参与者
BMI 为 28 至 35 kg/m²,且过去3-6个月内保持稳定(波动范围±5%)(基于受试者自述或医疗记录)
经研究者评估健康状况良好,根据研究前的病史、体格检查及临床实验室检查确定
⏩ 主要终点
发生不良事件的参与者比例
⏩ 次要终点
Cmax、AUClast及血清 INHBE 水平(猜测是把血清 INHBE 作为疗效预测 Biomarker)
精准减脂,
ARO-ALK7 能否塑造小蛮腰?
2024 年 8 月14 日,Arrowhead 在肥胖/代谢研发网络研讨会上首次介绍了 ARO-ALK7 的非临床研究结果,以及初步的临床研究计划。根据截至目前的调研,Arrowhead 显然做到了!
相对于2024年网络研讨会上公布的资料,本次结果主要更新了以下信息:
体重脂肪减少的可能机制
降低剂量后的食蟹猴药效学数据
饮食诱导的 DIO 小鼠模型的药理学研究
毒理试验的初步结果

ARO-ALK7 在饮食诱导的 DIO 小鼠模型中的药理学研究
☆ 沉默脂肪组织中 ALK7 抑制了 DIO 小鼠的体重增加并改善身体成分
18 周龄的 C57 雄性 DIO 小鼠接受每周 3mg/kg ARO-ALK7 治疗,研究结束时,与生理盐水对照组相比,给药组 DIO 小鼠腹股沟白色脂肪组织中 ALK7 mRNA 的表达量下调 80%,抑制了 40% 的体重增加;同时,通过 DEXA 成像分析,发现在保持瘦体重的前提下,脂肪含量减少了约 50%。
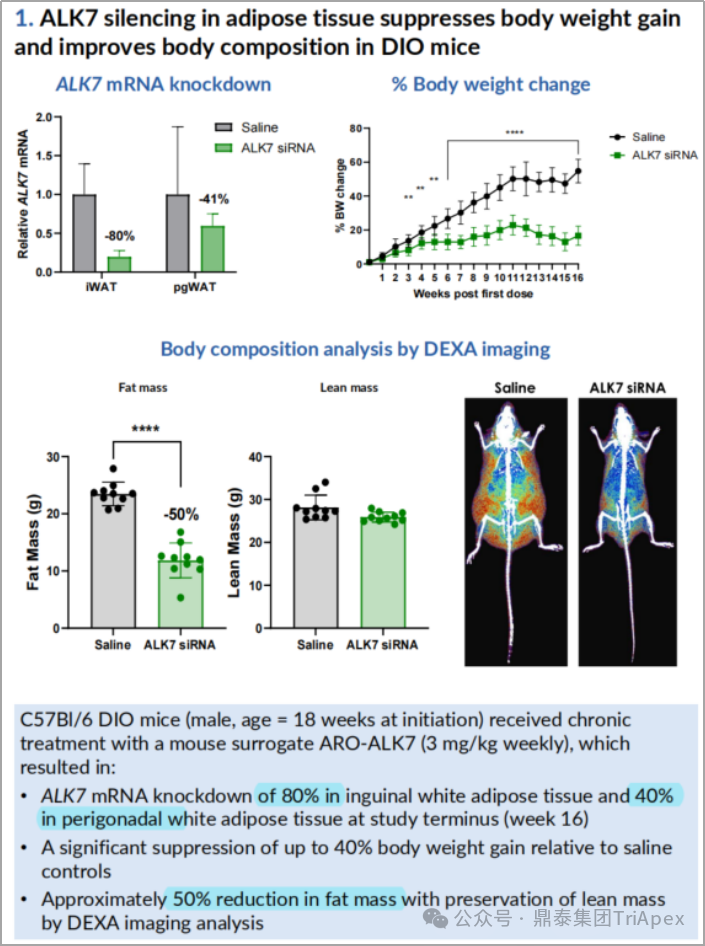
图10.沉默脂肪组织中 ALK7 抑制了 DIO 小鼠的体重增加并改善身体成分(资料来源:Arrowhead:Keystone Symposia on Obesity and Adipose,2025)
☆ 体重脂肪减少的机制:增强的脂肪降解和增加的能量消耗
分别在使用 β3-肾上腺素受体激动剂CL316243(腹腔注射,1 mg/kg)前和注射 30min 后收集血清:
ALK7 表达减少的动物(N=10)血浆中甘油、游离脂肪酸(NEFAs)和酮体水平升高(Mean±SEM),脂解基因(lipolytic genes)表达上调。
在第8周时,使用 TSE Phenomaster 系统对 C57BL/6 DlO小鼠(N=10)进行了能量消耗测量,ALK7 siRNA 组可见:
O2消耗量增加
热量产生增加
摄食情况没有变化
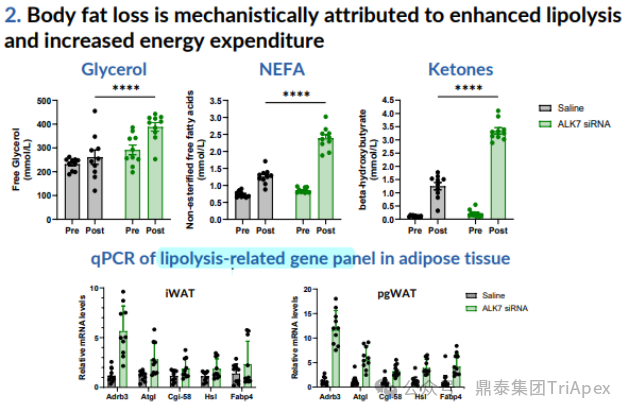
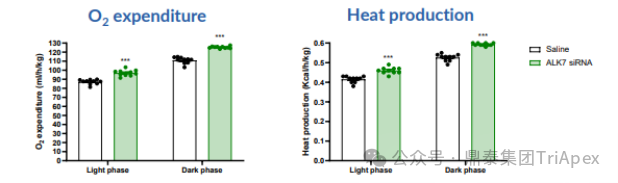
图11.体重脂肪减少的机制:增强的脂肪降解和增加的能量消耗(资料来源:Arrowhead:Keystone Symposia on Obesity and Adipose,2025)
♦ 对比替尔泊肽单一疗法,ALK-siRNA+替尔泊肽联用增强减重治疗获益
本试验共分为 4 组,分别为生理盐水对照组(QW),ARO-ALK7 siRNA组(3 mg/kg,QW),替尔泊肽(0.07mg/kg,QD)以及替尔泊肽(0.07mg/kg,QD)+ARO-ALK7 siRNA组(3mg/kg,QW)。动物给药时的起始年龄为 20 周龄,N=10。
主要研究结果如下:替尔泊肽和 ALK7 siRNA 联用对体重和脂肪量减少具有相加作用;ALK7 siRNA 改善了替尔泊肽单药治疗观察到的瘦体重损失。

图12. ARO-ALK7 与替尔泊肽联用,增强了替尔泊肽的减重效果(资料来源:Arrowhead:Keystone Symposia on Obesity and Adipose,2025)
ARO-ALK7 在非人灵长类动物中的药效学研究
♦ 单次 SC 给药可持续降低皮下脂肪组织中 ALK7 mRNA
在食蟹猴中评估了 ARO-ALK7 剂量范围为 0.1 - 0.75 mg/kg 的药效作用(N=4)。
单次给药后,脂肪组织中可见 ALK7 mRNA 剂量依赖性降低,起效剂量为 0.3 mg/kg
以 1.5 mg/kg 给药后,在腹腔脂肪组织中 ALK7 敲降约 75%,持续长达 12 周
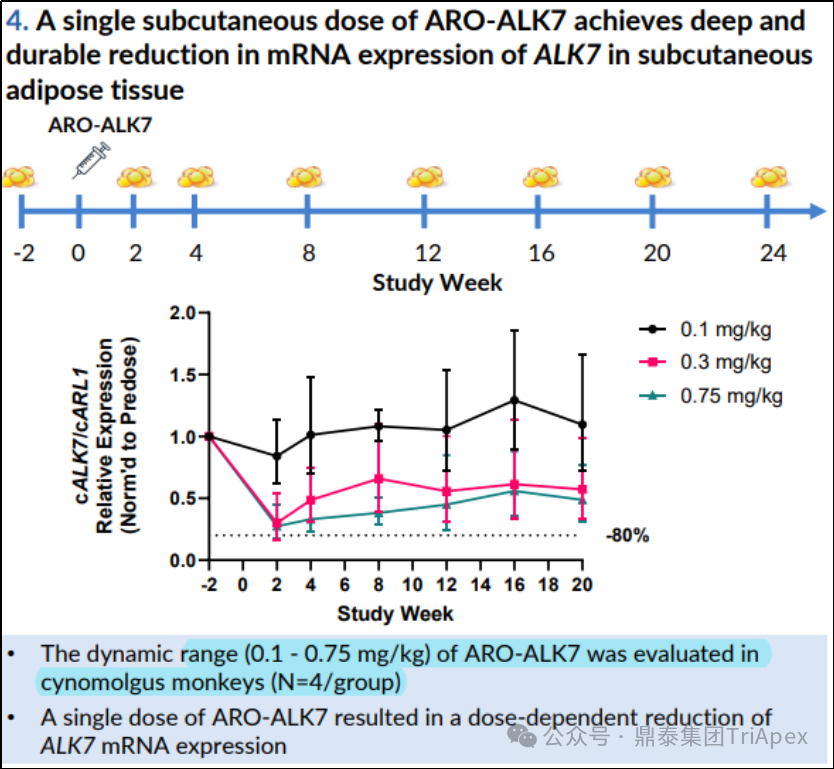
图13. 评估 ARO-ALK7 在食蟹猴中的剂量范围(资料来源:Arrowhead:Keystone Symposia on Obesity and Adipose,2025)
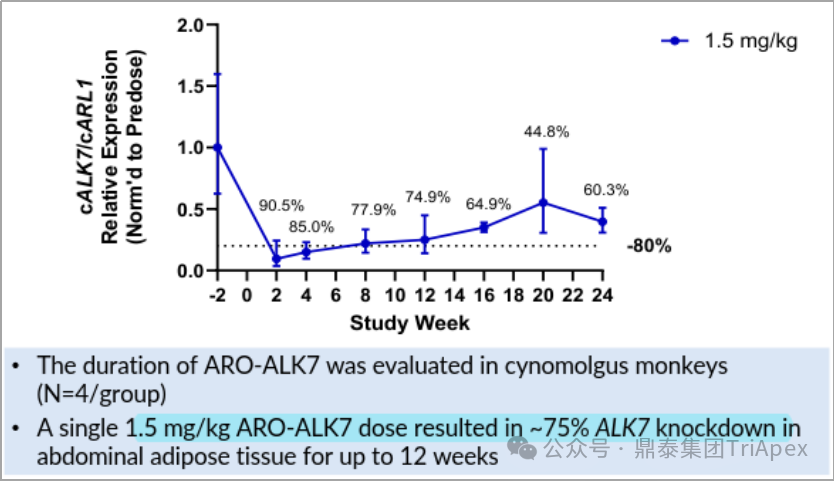
图14. ARO-ALK7 单次皮下注射,可实现持久的降低食蟹猴皮下脂肪组织中 ALK7 mRNA(资料来源:Arrowhead:Keystone Symposia on Obesity and Adipose,2025)
此前的实验结果显示,在 0.75~3 mg/kg 剂量下虽可见显著疗效但剂量反应关系不明显。根据 Arrowhead 在既往项目中的实践经验,可能会依据 0.1 mg/kg 或 0.3 mg/kg 作为起效剂量用于首次人体试验中起始剂量的设计依据(后续我们会持续关注)。
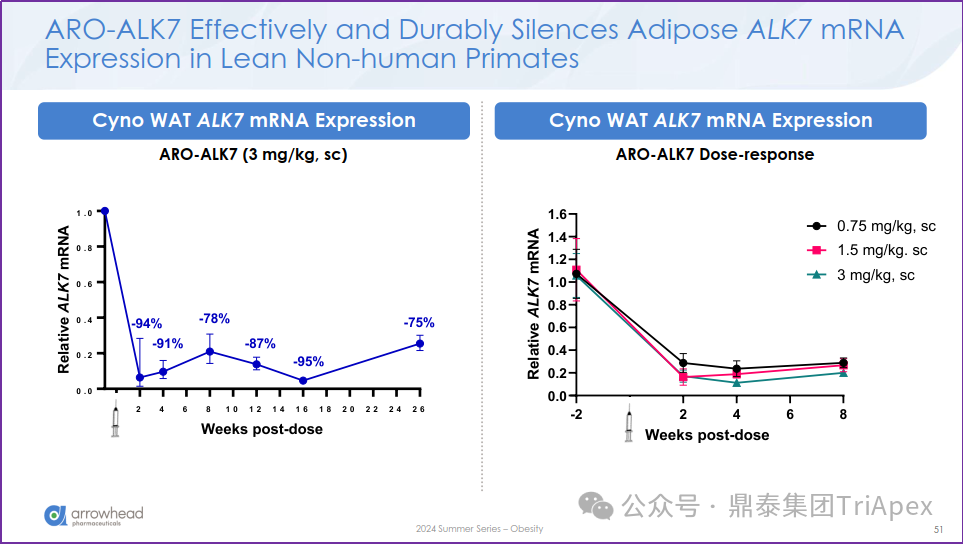
图15. ARO-ALK7 有效且持久地抑制瘦型非人灵长类动物的脂肪 ALK7mRNA 表达(资料来源:2024 Summer Series of R&D Webinars Part IV – Obesity Programs)
☆ ARO-ALK7 在大鼠中的毒理学研究
ARO-ALK7 以 30、60 或120 mg/kg(第15天进行解剖)单次给予 HAN WISTAR 大鼠,或在第1天和第 29 天以 60 mg/kg(第43天进行解剖)重复给药,耐受性良好。
组织病理学检查:注射部位/淋巴结出现空泡化巨噬细胞浸润(≥60 mg/kg);肝脏枯否细胞细胞肥大(≥30 mg/kg)
未发现不良或剂量限制性毒性

图16. ARO-ALK7 在大鼠中的毒理学研究(资料来源:Arrowhead:Keystone Symposia on Obesity and Adipose,2025)
☆ 临床试验设计
在 ALK7 siRNA 的角逐中,Arrowhead 也处于暂时领先的位。现已获得监管部门批准,在新西兰启动 I/IIa 期临床试验(ARO-ALK7-1001),预计将于2025年第二季度开始给药。

ARO-ALK7-1001 是一项 Phase I/IIa 期首次人体剂量递增研究,旨在评估 ARO-ALK7 在成人肥胖参与者(最多90名)中的安全性、耐受性、PK 和 PD,主要研究内容如下:
第一部分:用于评估 ARO-ALK7 单药治疗的单次和多次给药情况
第二部分:用于评估 ARO-ALK7 与替尔泊肽联合使用的情况
ARO-ALK7 目前尚处于早期临床开发阶段,基于 RNAi 的创新机制和非临床数据展现了其在减脂和保肌的双重潜力。尽管目前尚未公开关于 ARO-ALK7 更为详细的临床试验设计和试验结果的详细信息,但随着 2025 年临床试验的推进,该药物有望为肥胖治疗领域带来突破性的进展。我们期待着 Arrowhead Pharmaceuticals 在未来披露更多关于该药物的临床研究进展。
展望,方向与信念
GLP-1 受体激动剂(如司美格鲁肽、替尔泊肽)虽为肥胖症治疗带来革命性进展,但其肌肉流失等局限性逐渐显现。以 INHBE 和 ALK-7 siRNA 为代表的创新疗法,则如同划破寂静夜空的明星,通过增强脂肪降解、保护肌肉等机制,为这一领域开辟了全新的治疗思路。
从创新药物研发的历史经验来看,重大突破往往始于对关键机制的深入理解和精准干预。在减脂保肌领域,靶向调节能量代谢的关键节点基因,无疑为实现精准治疗提供了全新思路。这一治疗领域的持续变革,不仅有望重新定义肥胖症的治疗格局,更可能为代谢性疾病的整体防控带来颠覆性改变。
未来,鼎泰集团(TriApex)将持续关注 INHBE 和 ALK siRNA 相关研究进展,并与行业同仁共同携手探讨靶向治疗在脂肪管理中的更多可能性,共同为这一领域注入更强的续航力与生命力。
供稿:转化科学和药政策略部
参考资料:


































































































































