


在上期“燃烧我的卡路里”系列文章中,我们首先介绍了 INHBE 作为体重管理靶点的独特优势、鼎泰集团昆明科灵(KBI)针对靶向 INHBE 的体内药效学试验,以及如何与传统的降脂类动物实验进行差异化设计、在临床前动物实验阶段如何充分阐明 INHBE siRNA 的优越性等问题进行了探讨(《减脂保肌,INHBE 有态度,KBI 有招数》 点击查看原文)。
在“他山之石”系列文章中,鼎泰团队对已上市的用于治疗成人原发性高胆固醇血症(杂合子型家族性和非家族性)或混合型血脂异常患者的治疗及杂合子家族性高胆固醇血症(HeFH)或临床动脉粥样硬化性心血管疾病(ASCVD)的 siRNA 药物 —— Inclisiran(Leqvio®,点击查看原文)的上市历程及临床开发路径进行了复盘分析,并对与临床转化有关的内容进行了总结。Inclisiran 的上市,证明了寡核苷酸药物在慢病领域的潜力,掀开了 siRNA 药物用于慢病治疗的新篇章,也引领了更多 siRNA 候选分子在代谢性疾病等领域的开发。目前,已有多种靶点、多款 siRNA 和 ASO 药物被开发用于高血脂、高血压、高血糖等的治疗,一场全新的慢病治疗药物的研发竞赛已开启。

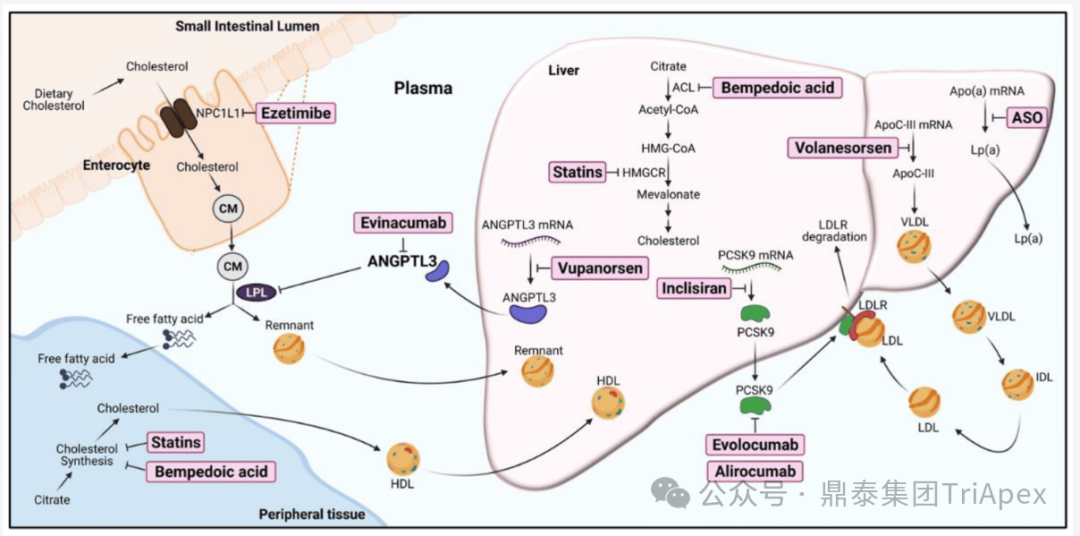
用于血脂管理的在研和已上市药物[1,2]
最近,血管生成素样蛋白家族成员血管生成素样蛋白3(angiopoietin-like 3,ANGPTL3)被证明可抑制 LPL 活性,并参与脂蛋白代谢的调节,成为治疗血脂异常的一个有前景的药理学靶点。本期内容将介绍 ANGPTL3 的相关信息,并对正在进行 Ⅱ 期临床的 siRNA 药物 Zodasiran 的临床开发路径进行介绍。
全文共:10703 字 16 图
预计阅读时长:25分钟
ANGPTL3 生物学背景
血管生成素样蛋白(ANGPTL)是一个分泌型糖蛋白家族,由 8 个成员(ANGPTL1-8) 组成。ANGPTL 与血管生成素具有高度同源性,后者是血管生成的关键调节因子。ANGPTL3 由 460 个氨基酸组成,分子量约为 70kDa,主要由肝脏表达和分泌。
根据 NCBI Blast 氨基酸序列比对, ANGPTL3 在人和小鼠、大鼠、犬、食蟹猴、黑猩猩间的同源性(Identities)分别为 77%、79%、88%、97%、99%。除黑猩猩外,与人的同源性最高的是食蟹猴。以上信息有助于了解靶向 ANGPTL3 的 siRNA 的相关种属。
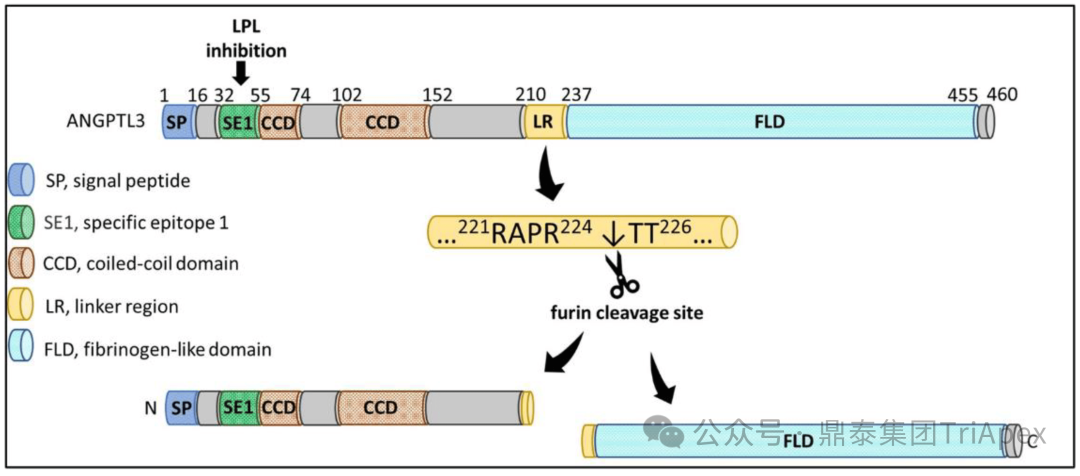
ANGPTL3 蛋白的结构特征[2]
■ ANGPTL3 可通过多种途径参与脂质代谢:
(i)促进极低密度脂蛋白(VLDL)的分泌;抑制 ANGPTL3 可以可减少 VLDL 的分泌;
(ii)抑制脂蛋白脂肪酶(LPL),从而调节甘油三酯(TG)的血管内清除率,提高 TG 水平。抑制 ANGPTL3 可以可降低血清中 TG 水平;
(iii)控制低密度脂蛋白胆固醇(LDL-C)的产生和清除[2]。抑制 ANGPTL3 导致血浆 LDL-C 水平降低,可能的原因是抑制 ANGPTL3 促进了VLDL清除或减少 VLDL 分泌,从而减少 VLDL 向 LDL 的转化[2];
(iv)抑制内皮脂肪酶(EL),后者参与高密度脂蛋白胆固醇(HDL-C)和 VLDL-C 的分解代谢。抑制 ANGPTL3 可以有效增强 EL 活性,降低 HDL-C 和 VLDL-C 水平。
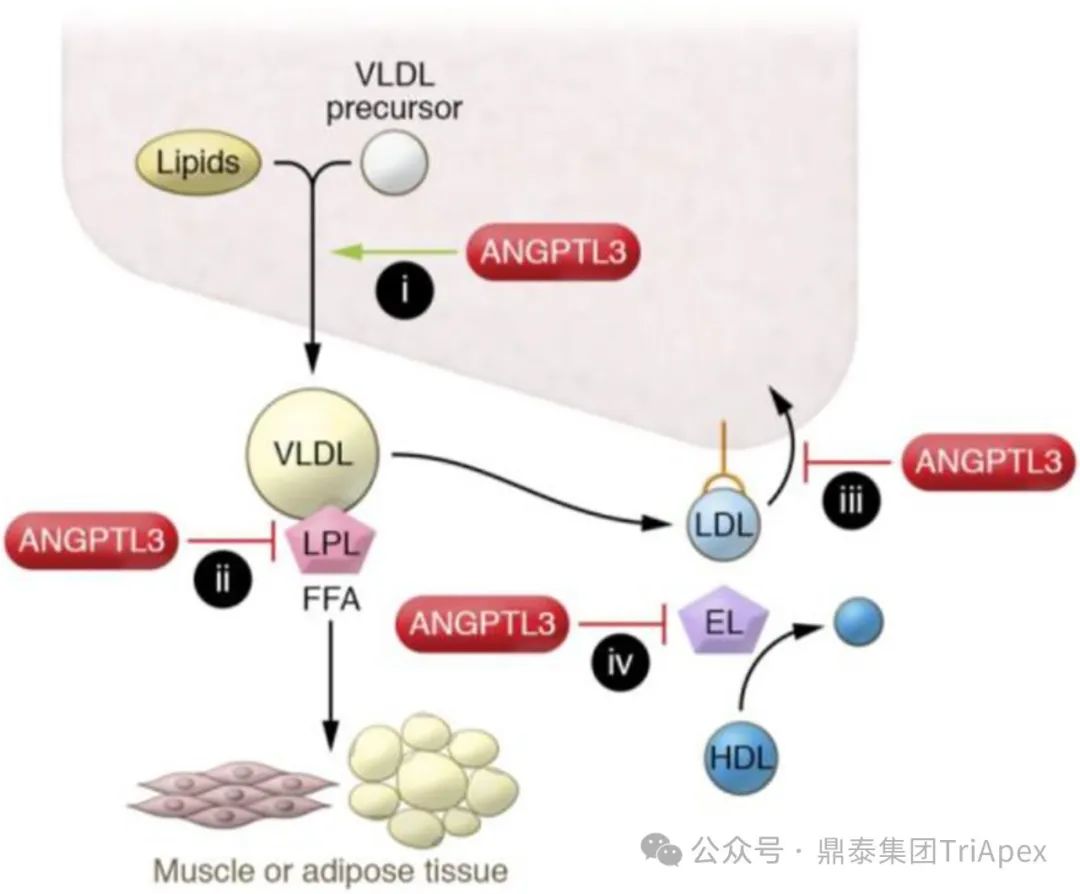
ANGPTL3 在脂蛋白代谢中的作用[3]
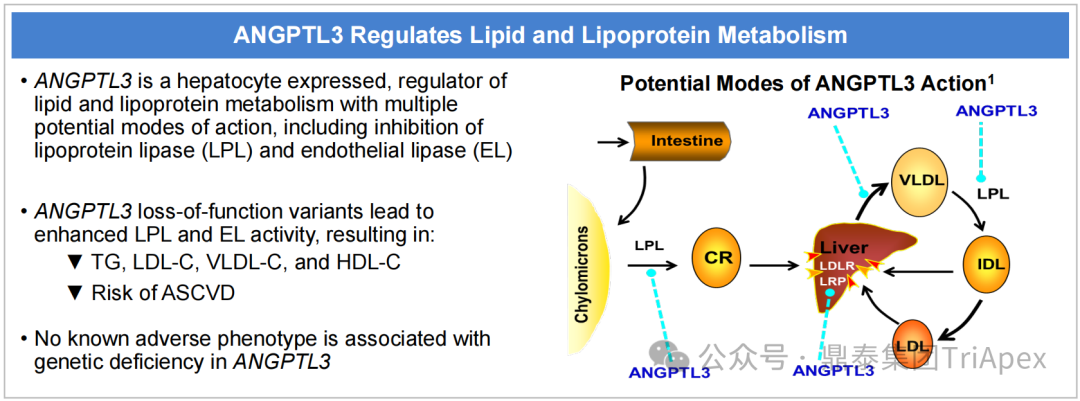
ANGPTL3 调节脂质和脂蛋白代谢[4]
人类 ANGPTL3 纯合功能缺失突变会导致家族性混合型低脂血症,其特征是 TG、LDL-C 和 HDL-C 浓度降低。杂合子携带者患冠状动脉疾病的风险比非携带者低 34-39%,且无明显的不良临床表型。尽管 HDL-C 降低, ANGPTL3 功能缺失变体 variant 似乎对动脉粥样硬化性心血管疾病(ASCVD)具有保护作用[5]。单抗 Evinacumab 和反义寡核苷酸 Vupanorsen 通过抑制 ANGPTL3 可复制 ANGPTL3 功能缺失携带者的表型。但抗体需每月或更频繁地静脉给药,影响对治疗的依从性;Vupanorsen 由于 ALT 和肝脂肪变性增加,已经停止。
对于以 ANGPTL3 为靶点的 siRNA 药物的开发,国内外多家公司积极布局。其中,Arrowhead 的 Zodasiran(ARO-ANG3)进展较快,现已进展到临床 Ⅱ 期。本期内容将结合鼎泰团队的项目经验,对 Zodasiran 的临床内容进行整理,以期对 ANGPTL3 siRNA 药物的非临床研究和临床开发思路提供参考。
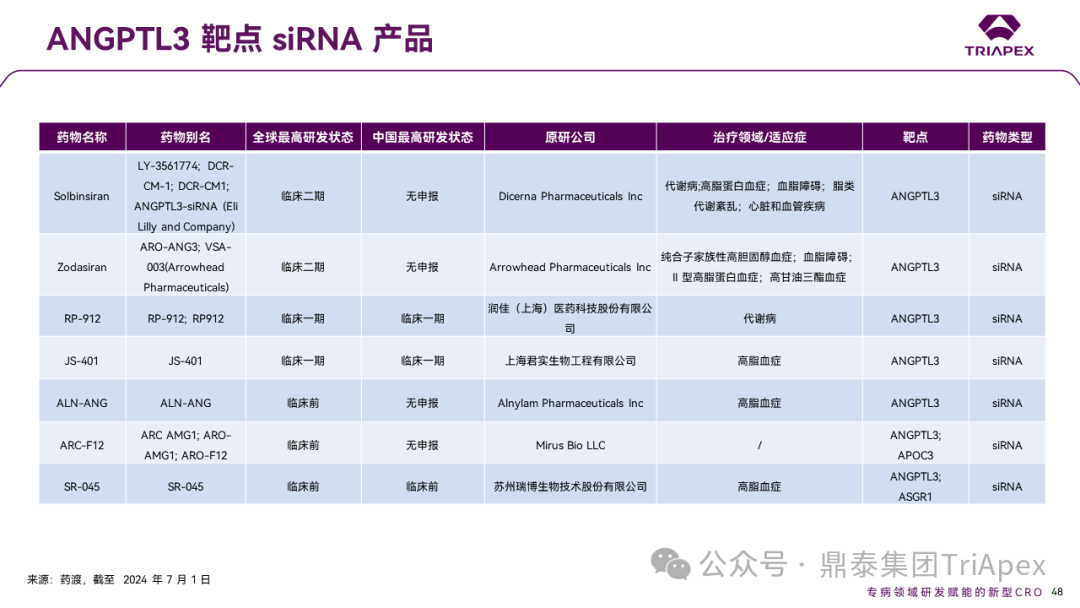
ANGPTL3 靶点 siRNA 产品
Zodasiran 产品信息
Zodasiran(ARO-ANG3)是 Arrowhead Pharmaceuticals 研发的以 ANGPTL3 为靶点的双链小干扰 RNA (siRNA)分子,通过 GalNac 载体结合靶向肝细胞,可降解细胞质内的 ANGPTL3 mRNA,ANGPTL3 蛋白表达的减少预计会导致 LDL、HDL-C、TG 和 ApoB 的相应减少。动物研究表明,ARO-ANG3 能高效抑制 ANGPTL3 mRNA 和 ANGPTL3 蛋白的表达,引起 TG、LDL-C 和 HDL-C 的相应降低。在野生型小鼠、正常饮食食蟹猴和各种血脂异常动物模型中评价了 ARO-ANG3 的临床前药理作用。
在小鼠中,ARO-ANG3 治疗导致血清 ANGPTL3 蛋白水平显著降低,与血清 TG 降低和血清 HDL 升高相关联。
在食蟹猴中,接受两次 Q4W 3 mg/kg 剂量 ARO-ANG3 治疗的动物血清 ANGPTL3 的最大降幅约为 90%[6]。
在人上,这种作用可能会降低 ASCVD 的风险,特别是在缺乏 LDLR 活性的患者(如纯合子家族性高胆固醇血症)或混合性血脂异常患者中。
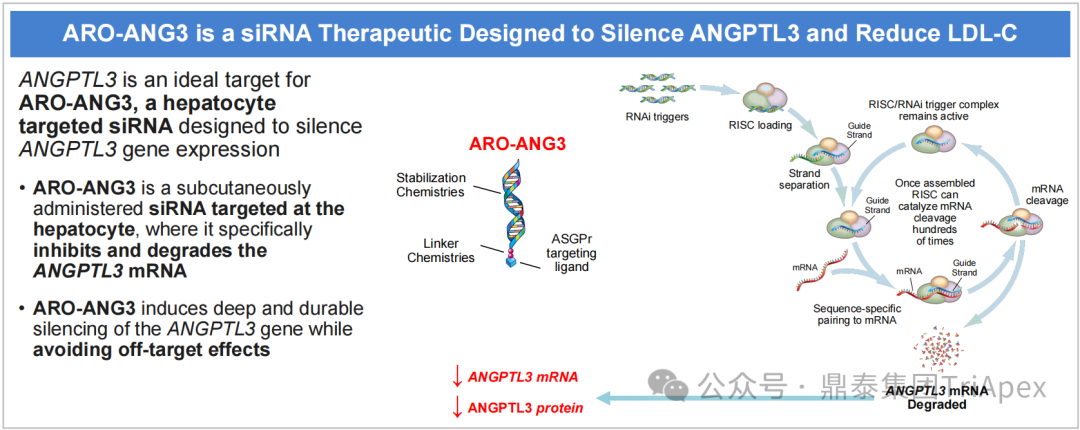
Zodasiran 作用机理示意图[4]
■ Zodasiran 临床开发路径
截至目前,Zodasiran 已进展到临床 Ⅱ 期,针对不同适应症开展了 2 项 Ⅱ 期临床试验。
Ⅰ 期临床试验(NCT03747224)为篮式试验,主要目的是评估 Zodasiran 在健康受试者和血脂异常患者中的安全性和耐受性。
Ⅱ 期临床试验(NCT04832971)主要目的是评估 Zodasiran 治疗后血脂异常患者空腹 TG 变化。
Ⅱ 期临床试验(NCT05217667)主要目的是评估 Zodasiran 治疗后纯合子家族性高胆固醇血症患者空腹 LDL-C 变化。
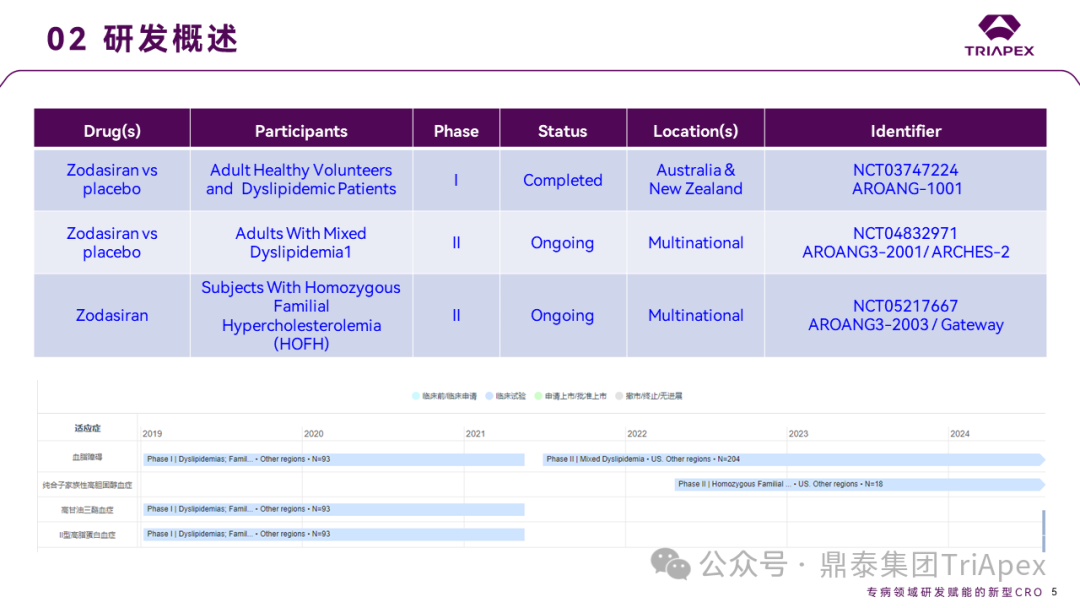
Zodasiran临床试验概览
1
Ⅰ 期临床试验
(NCT03747224/ AROANG1001)
在这项概念验证试验中,采用篮式试验设计,初步评估 ARO-ANG3 在健康受试者和患有各种血脂异常受试者中的安全性、耐受性、药代动力学和药效学。

Ⅰ 期临床试验基本信息
在剂量递增部分(队列1至4),剂量递增需要数据安全委员会(DSC)根据先前队列的安全性数据批准,并且至少在当前健康受试者(NHV)队列的第 8 天。基于至第 8 天的可用安全性数据,DSC 将投票批准开放下一个计划队列/剂量水平的入组。DSC 决策将基于所有可用的总体安全数据,包括至少到当前队列第 8 天的所有可用数据。剂量递增直至 300mg 剂量水平完成,或者由于安全或其他原因由 PI、DSC 或申办方提前停止试验。
队列 9 仅对完成队列 7、7b 和 7c 的患者开放。在队列 7、7b 和 7c 的研究结束时,患者可以选择继续进行 End of Study 访视或继续接受队列 9 中每 12 周(Q3M)给药,最多给药 4 次。
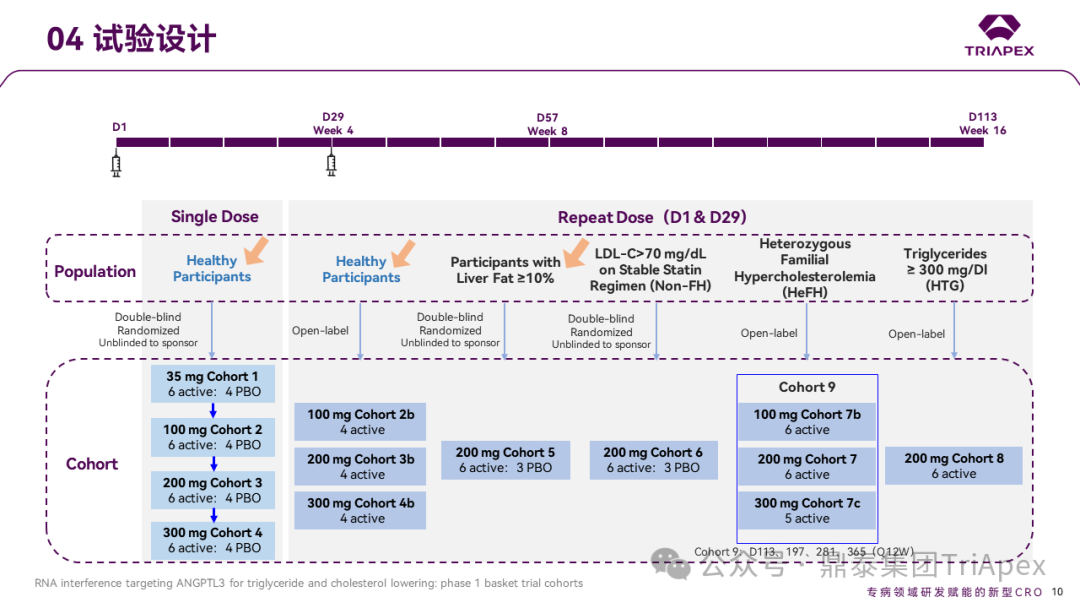
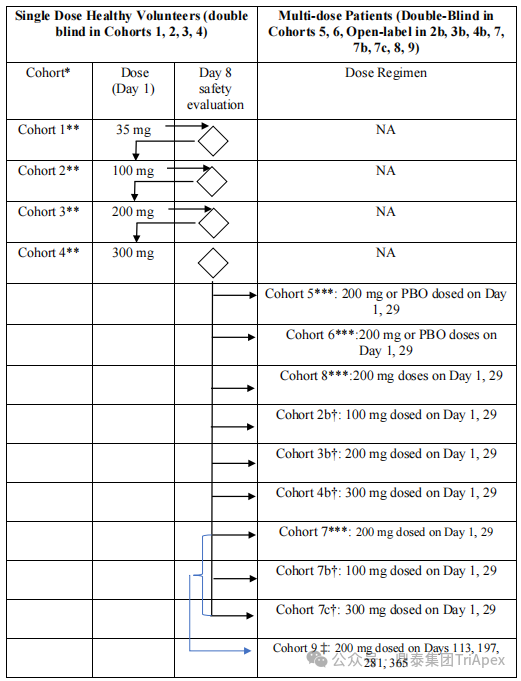
Ⅰ 期临床试验设计[6]
已发表文献中报告了单次和多次递增剂量的 ARO-ANG3 在健康受试者中的安全性、耐受性和药效学效应的关键结果。鉴于此前针对 ANGPTL3 的 ASO 疗法(Vupanorsen)曾报道了与转氨酶和肝脏脂肪增加,本研究还报告了一项重复给药队列的结果,评估了 ARO-ANG3 在基线肝脂肪变性受试者中的疗效。
在健康受试者 SAD 队列中,24 名受试者接受 ARO-ANG3 35mg(队列1)、100mg(队列2)、200mg(队列3)或300mg(队列4)皮下注射,16 名受试者在第 1 天接受安慰剂(队列1-4)。
在健康受试者 MAD 队列中,12 名受试者在第 1 天和第 29 天接受 ARO-ANG3 100mg(队列2b)、200mg(队列3b)或300mg(队列4b)。
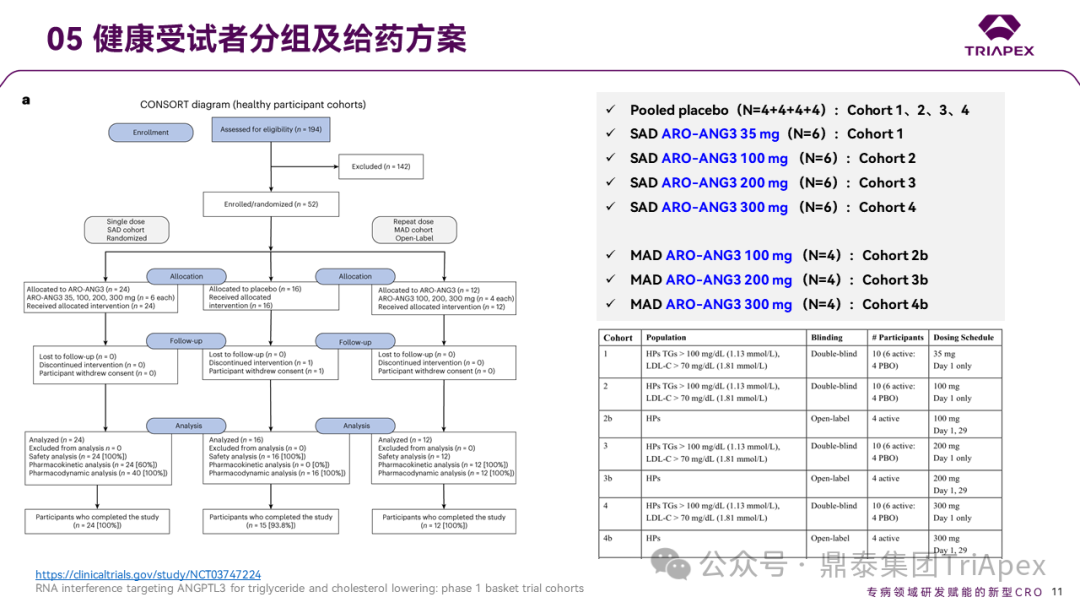
健康受试者分组及给药方案
在肝脂肪变性队列中(队列5),6 名受试者在第 1 天和第 29 天接受 ARO-ANG3 200mg,3 名受试者接受安慰剂。该队列的受试者需要具有基线肝脂肪变性,定义:通过磁共振成像估计的质子密度脂肪分数 (MRI-PDFF)进行测量的肝脏脂肪含量为 ≥10% 。
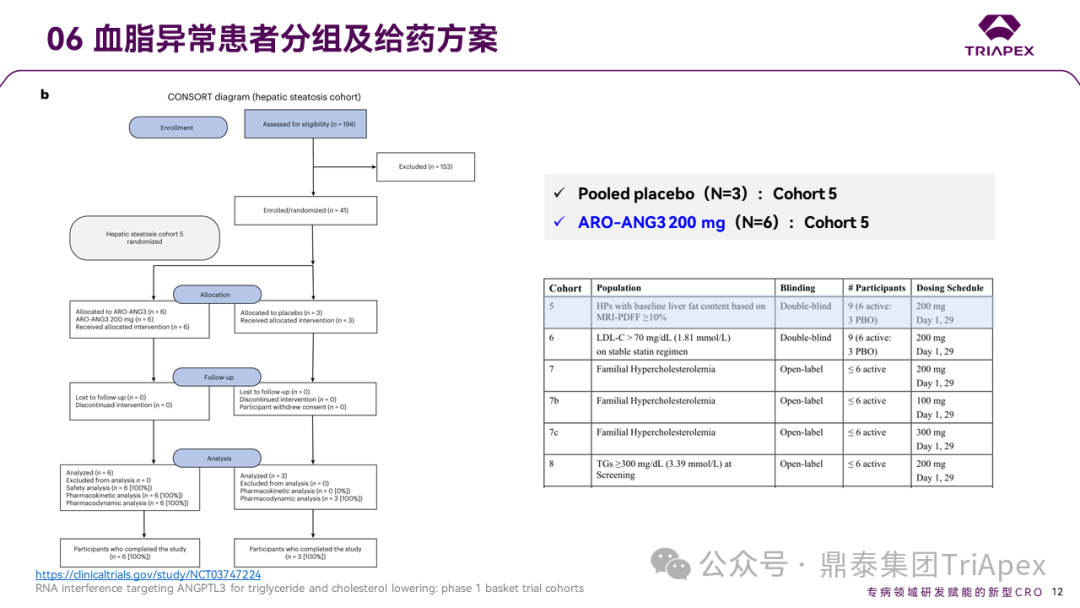
血脂异常患者分组及给药方案
■ FIH起始剂量设计依据[6]:
◆ 指导原则考虑
根据 EMA 指南(2017),建议采用最相关动物种属中的 NOAEL 计算健康受试者 MRSD【实际未采用】
根据 FDA 指南(2005),建议采用最敏感动物模型中的 NOAEL 计算健康受试者 MRSD【实际未采用】
◆ 行业共识
对于寡核苷酸药物,安全窗的计算更适合采用非人灵长类 NOAEL
◆ 换算依据
寡核苷酸药物种属间换算:根据报道,最合适的方法是基于 mg/kg,而非 BSA(mg/m2)或血浆暴露量(AUC 或 Cmax)(Yu et al. 2001)
寡核苷酸药物的 HED:可基于 mg/kg 剂量按照 1:1 直接从猴外推到人体 (Yu et al . 2015)
其他 siRNA 的经验:ARO-HBV (2018.3) 和 ARO-AAT (2018.3) 的 FIH 试验中,使用 1:1 mg/kg 缩放因子基于猴 NOAEL 确定起始剂量
◆ 药效学终点
与小鼠、大鼠和猴 mRNA 具有交叉反应性
野生型小鼠中,ARO-ANG3 组血清 ANGPTL3 蛋白水平显著降低,与血清 TG 降低和 HDL 升高相关联;起效剂量为 0.5mg/kg
在食蟹猴中,ARO-ANG3 以 3mg/kg Q4W 给药 2 次,血清 ANGPTL3 最大降幅约为 90%
其他血脂异常小鼠和猴模型数据(未详细披露)
◆ 推荐的最大起始剂量
本研究中建议的健康受试者起始剂量为 35mg,推测是基于小鼠起效剂量 0.5 mg/kg 确定(0.5 mg/kg *70 kg = 35 mg)
◆ 安全系数计算
根据 GLP 毒性研究,根据猴和大鼠 NOAEL (300mg/kg 和 15 mg/kg)计算的安全系数为 600 和 30(基于 BW,按 70kg 计)
◆ 最大递增剂量
研究中建议的最大剂量为 300mg
根据猴 NOAEL,安全系数为 70
◆ 剂量扩展
Cohort 5、6、7 和 8 组使用的建议剂量为 200mg,依据如下:35、100、200 和 300mg 剂量下安全性相当;200mg 以上剂量,血清 ANGPTL3 和血清 TG 的减少达到平台



剂量设计依据
结果显示,ARO-ANG3 在健康受试者和肝脂肪变性患者中均耐受良好:
没有死亡、危及生命的 TEAE 或导致任何受试者停药或提前退出研究的 TEAE;没有与治疗相关的 SAE,大多数 TEAE 为轻度或中度。
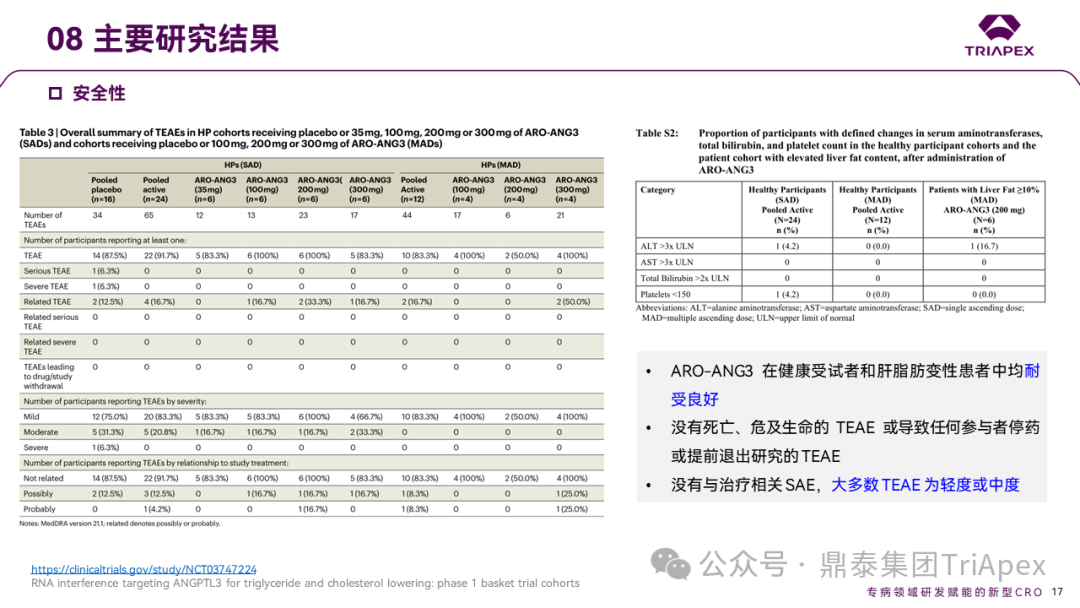
Ⅰ 期临床试验安全性相关结果
药代动力学特征显示 ARO-ANG3 在健康受试者中的全身吸收快速且持续, Tmax 为 6.0 ~10.5 h。给药后 24~48 h,ARO-ANG3 从血浆中清除,t1/2为 3.9 h~6.6 h。

Ⅰ 期临床试验药代动力学相关结果
多个队列的结果表明,在健康受试者中单次或重复给药 ARO-ANG3 以及肝脂肪变性受试者队列中重复给药后,在至少 12 周内具有强大、一致且持久的药效学效果。对最后一次给药后 12 周的关键药效学和脂蛋白水平数据进行了汇总,包括 ANGPTL3、TG、non-HDL-C、VLDL-C、LDL-C、HDL-C 和 ApoB。
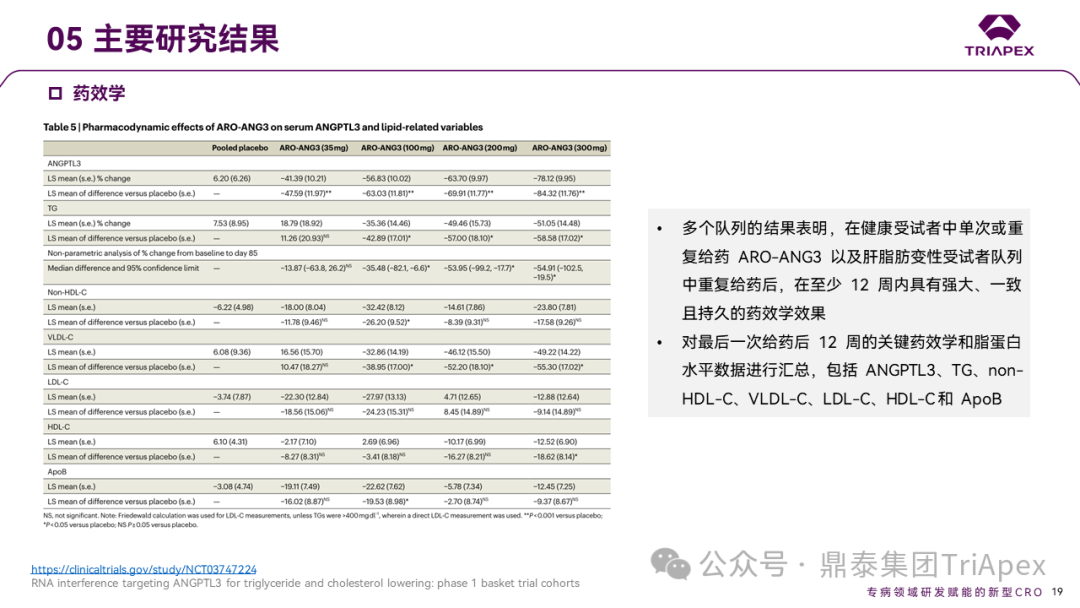
Ⅰ 期临床试验药效学相关结果
在健康受试者 SAD 研究中,D3 开始血清 ANGPTL3 浓度降低,在单次给药后 2~6 周达到最大平均降低,且 ANGPTL3 水平以剂量依赖方式降低。
D85 时,与基线相比,35mg 和 300mg 剂量组 ANGPTL3 的平均百分比变化分别为 -44.7% 和 -77.8%。与此相对,安慰剂组增加了 6.4%。此外,ARO-ANG3 可不同程度地降低健康受试者的 TG(8.7%~51.7%)、VLDL-C(8.8%~51.7%)、non-HDL-C(17.5%~28.7%)、LDL-C(4.1%~26.8%)、ApoB(6.7%~23.1%)和 HDL-C(2.4%~12.9%)水平[5],个别指标未见明确的剂量相关性。
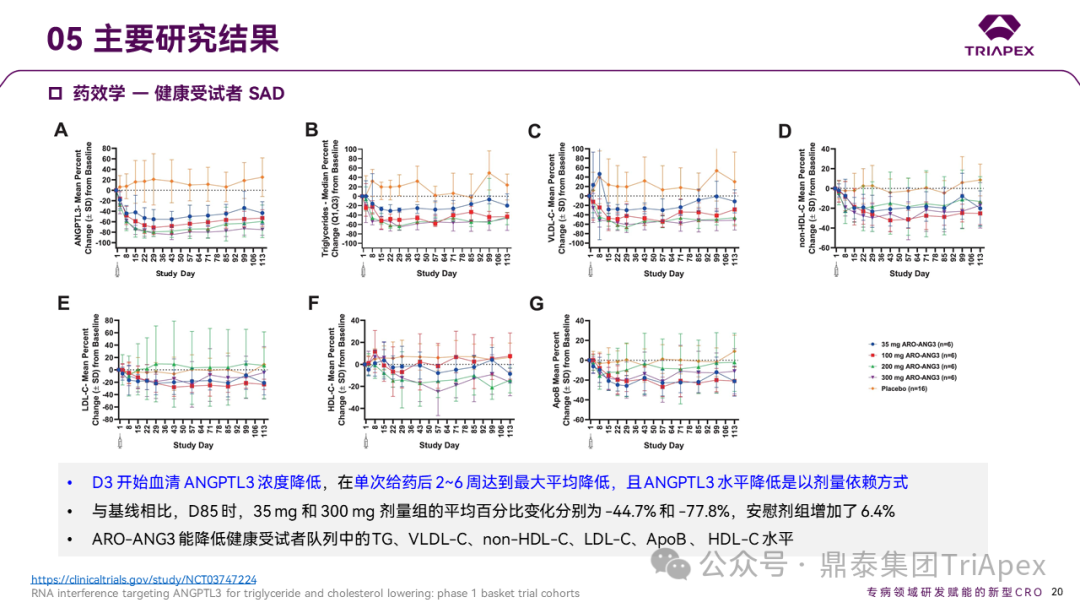
Ⅰ 期临床试验药效学相关结果
在健康受试者 MAD 研究中,重复给药 ARO-ANG3 显示出与单次给药类似的药效学参数变化。由于未设置安慰剂对照组,与 SAD 队列中安慰剂组的数据进行了比较。ARO-ANG3 给药可在 D3 开始降低 ANGPTL3 浓度,并且呈剂量依赖性。D113时,与基线相比,100mg 和 300mg 剂量组的平均百分比变化分别为 -64.4% 和 -92.7%,而安慰剂的平均百分比增加了 25.0%。重复给药 ARO-ANG3 也能显著降低 TG、non-HDL-C、VLDL-C、LDL-C、HDL-C 和 ApoB 水平,个别指标的变化未见明确剂量依赖性。
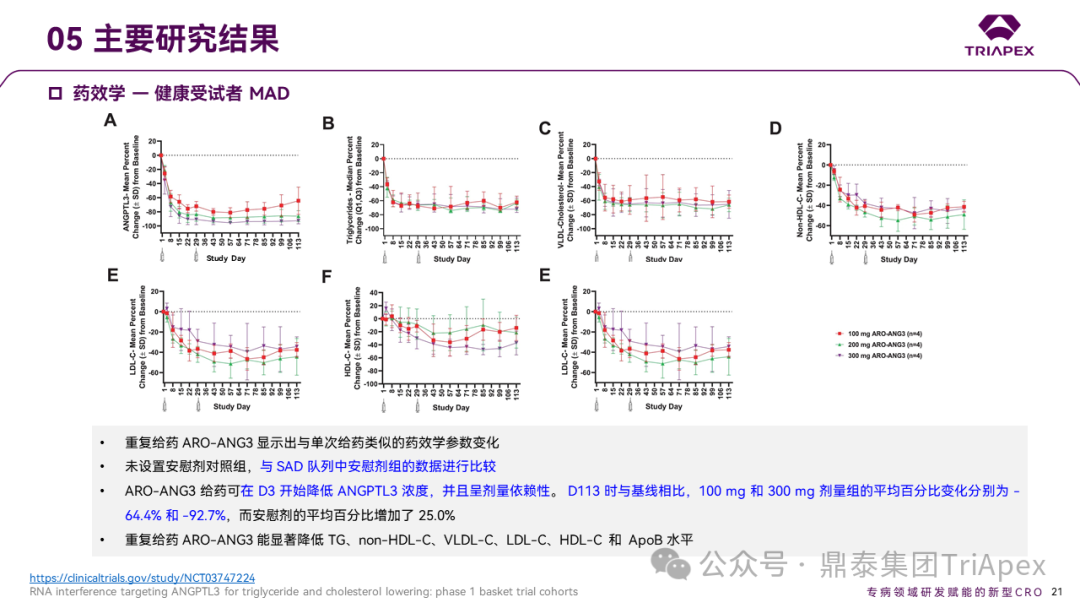
Ⅰ 期临床试验药效学相关结果
在肝脂肪变性患者中, D113 时 ANGPTL3 与基线相比的平均百分比变化为 -85.3%,而安慰剂组增加了 13.0%。肝脂肪变性受试者治疗后 TG、non-HDL-C、VLDL-C、LDL-C、HDL-C 和 ApoB 水平降低。

Ⅰ 期临床试验药效学相关结果
本项 FIH、Ⅰ 期、随机、安慰剂对照、开放标签试验在四组(52名)健康受试者和一组(9 名)肝脂肪变性患者中研究了单次和重复 ARO-ANG3 给药的安全性、药代动力学和药效学。
ARO-ANG3 总体耐受性良好, ARO-ANG3 组和安慰剂组治疗中出现的 AE 频率相似。健康受试者对 ARO-ANG3 的全身吸收快速且持续,平均 Tmax 6.0~10.5h,给药后 24~48h 内从血浆中清除。健康受试者中, ARO-ANG3 治疗在给药后 85 天 ANGPTL3 显著降低;TG 和 non-HDL-C浓度在三个高剂量下均有所降低。这些数据支持 ANGPTL3 作为 ASCVD 治疗的潜在治疗靶点。
2
Ⅱ 期临床试验(NCT04832971)
本项 Ⅱ b 期、双盲、随机、安慰剂对照试验评估了 Zodasiran 在混合性高脂血症成年患者中的效果。

Ⅱ 期临床试验设计
受试者在知情同意后,至少 2 周稳定饮食,4 周稳定的最佳他汀类药物治疗(除非受试者他汀类药物不耐受)。符合标准的受试者以 3:1 的比例随机分配,接受 ARO-ANG3 给药(50、100或200 mg)或安慰剂。在双盲治疗期间,每位受试者将在第 1 天和第 12 周接受 2 次 SC 注射(Q3M)。所有剂量组将平行入组。入选的受试者需在整个研究过程中保持稳定的背景药物和指定的饮食。
36 周的双盲治疗期完成后,受试者可继续进行 24 个月的 OLE 治疗期,以评估混合血脂异常受试者长期给药 ARO-ANG3 的有效性、安全性和耐受性。双盲期 50 和 100mg 剂量组的受试者在 OLE 治疗期间继续接受相同剂量的 ARO-ANG3。200mg 剂量队列在下一次给药时过渡到 100mg 剂量组。OLE 治疗期受试者按指定剂量每季度给药(Q3M),直到选择出最合适的剂量。

Ⅱ 期临床试验设计
根据当前发布数据,50、100 或 200mg 队列实际入组人数分别为 50、51 和 52,安慰剂组为 51。主要研究终点为随机分组 24 个月时,进行 MRI-PDFF 检查,并测定空腹状态下 TG 相对于基线的变化率。
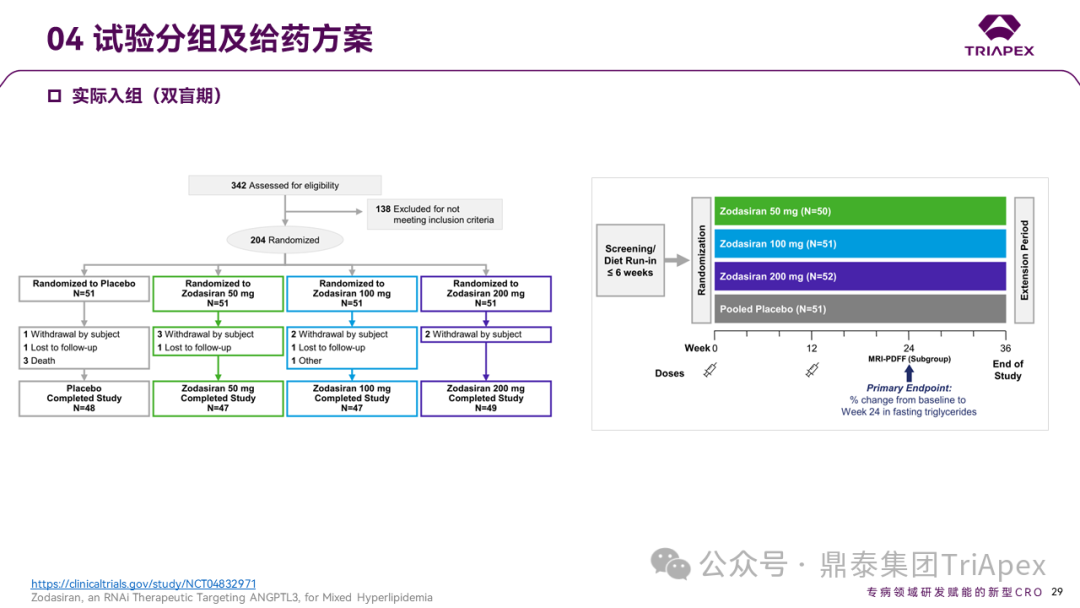
Ⅱ 期临床试验设计[7]
■ 剂量设计依据[8]:
选择剂量主要依据 AROANG31001 Ⅰ 期临床研究的单次剂量递增和多次剂量递增部分以及建模和模拟分析,最终选择 50、100 和 200mg 的剂量水平用于该研究。
在健康受试者 ARO-ANG3 的 Ⅰ 期研究中,35、100、200 或 300mg 的单次和多次给药(D1 和 D29)持续降低血清 TG 水平,直至第 12 周。单次给药200 和 300mg 组在第 12 周时 TG 比基线降低 50% 以上。在多次给药组中,100、200 和 300mg 剂量组在第 16 周(D113)保持 TG 降低 > 60%。ANGPTL3 的剂量反应更明显,呈剂量依赖性降低。与安慰剂相比,所有 3 种剂量水平都是有效的,并且降低了血清 ANGPTL3 和 TG。
基于 AROANG1001 研究中 93 名受试者血清 ANGPTL3、TG、LDL-C 和 non-HDL-C 水平,建立了 ARO-ANG3 的探索性群体动力学 -PD(popPK-PD)模型。根据模型的 PD 模拟预测,对于3种脂质生物标志物,从 100mg 开始,剂量饱和明显,预计从 200 和 300mg 开始,疗效改善很小。预计每季度给药方案(Q3M)可产生深度且一致的降脂效果。基于对基本完成和正在进行的 AROANG1001 研究的安全性审查,50、100 和 200mg 剂量选择安全,可以在更多血脂异常人群中进行研究。在 AROANG1001 研究中,在健康志愿者中观察到血脂降低方面的部分缓解,并且基于模型的 PD 模拟预测 50mg 是有效剂量。
假设以受试者平均体重为 70kg 转换,50 mg、100mg 和 200mg 分别约为大鼠 4 周/3 次 GLP 毒理学研究中 NOAEL (15 mg/kg)的 1/20、1/10和1/5;分别为猴4周/3次GLP毒理学研究中 NOAEL(300 mg/kg)的 1/420、1/210 和 1/105。本研究的剂量频率仅为每 12 周一次,而毒理学研究(6 个月大鼠和 9 个月猴)为每 4 周一次。因此,在临床计划剂量和动物毒理学研究 NOAEL 之间存在很大的安全范围。
综上,AROANG1001 提供的安全性数据 100 或 200mg 剂量水平的安全性特征没有明显差异。此外,预计 50mg 剂量水平的安全性特征与 Ⅰ 期研究相当。


Ⅱ 期临床试验剂量设计依据
结果表明,在第 24 周,与安慰剂相比,50、100、300mg组 TG 相对于基线的变化分别为 -51%、-57%,和 -63%;36 周时(试验结束)与安慰剂相比,变化分别为 -34%、-38% 和 -51%。

Ⅱ 期临床试验药效学研究结果
ANGPTL3 水平剂量依赖性降低(与安慰剂相比,50、100、200mg组分别为 -54%、-70%,-74%),与 TG 水平密切相关(Pearson 相关系数为 0.69)。平均 ANGPTL3 水平的剂量依赖性降低一直维持到试验结束(36 周,最后一次给药后 24 周),与安慰剂相比变化差异为 -45%、-57% 和 -64%。
此外,在所有三个剂量水平下还观察到其他致动脉粥样硬化脂蛋白参数的变化:在第 24 周, 200mg 剂量组的变化为 LDL-C(-20%),non-HDL-C(-36%),ApoB(-22%),HDL-C(-25%)。

Ⅱ 期临床试验药效学研究结果
与 ANGPTL3 水平一样,残余胆固醇水平的变化与 TG 水平的变化一致:从基线到第 24 周,与安慰剂相比,平均残余胆固醇水平相对于基线的差异为 -73%,-76% 、-82%,36 周时为 -43%、-45% 和 -58%;残余胆固醇水平的变化程度与 TG 水平的变化程度相关(Pearson相关系数为 0.87)。脂蛋白(a)与安慰剂相比,100mg 组在 24 周时的变化差异为 -20 %。
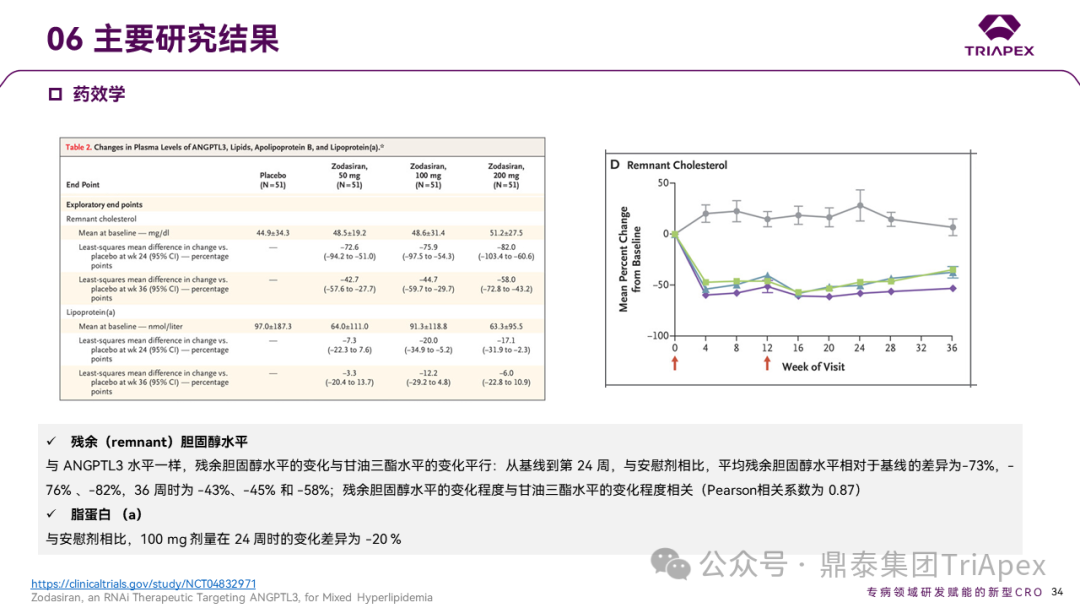
Ⅱ 期临床试验药效学研究结果
Zodasiran 在混合性高脂血症患者中安全性良好。TEAE 在治疗组和安慰剂组之间总体平衡。实验室安全性评估未发生有临床意义的变化,平均血小板计数未发生变化,HbA1c 有小幅变化。
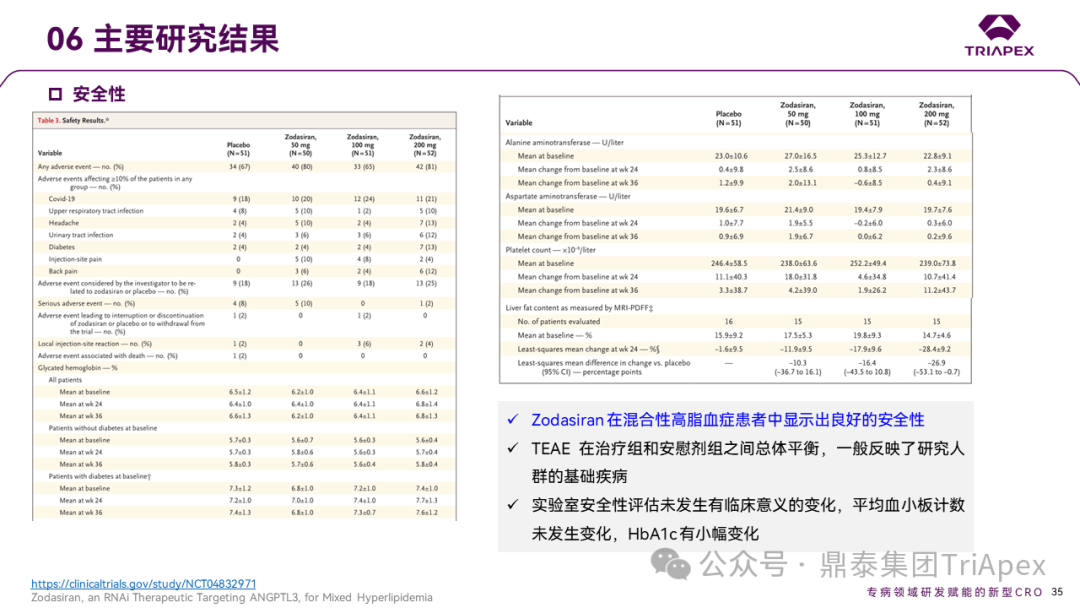
Ⅱ 期临床试验药效学研究结果
综上, Zodasiran 给药在 24 周内 ANGPTL3 水平相对于基线有显著的剂量依赖性下降;TG 水平显著剂量依赖性降低;富含 TG 的脂蛋白残留物和总致动脉粥样硬化脂蛋白(包括 LDL-C)水平持久降低。表型模拟了 ANGPTL3 功能失活突变对致动脉粥样硬化脂蛋白水平的影响。表明每季度给药 200 mg Zodasiran 的总体安全性和有效性特征,支持进一步研究。
3
Ⅱ 期临床试验
(NCT05217667/GATEWAY)
ARO-ANG3 2003 GATEWAY 研究是一项 Ⅱ 期开放标签研究,旨在评估 18 例 HoFH 患者 Q12W 给药 200mg 和 300mg ARO-ANG3 的有效性、安全性和耐受性。初始治疗期长达 36 周,可选择 24 个月的延长治疗期。研究的主要终点是 LDL-C 相对基线变化的百分比。

Ⅱ 期临床 GATEWAY 试验设计
试验纳入 18 名纯合子家族性高胆固醇血症患者(HoFH),以 1:1 的比例随机接受 200 或 300mg ARO-ANG3。在初始 36 周,受试者在第 1 天和第 84 天(12周)接受 200 或 300mg ARO-ANG3 共 2 次(Q3W)。在OLE期,受试者在第 1 天和第 3、6、9、12、15、18、21 个月接受 200 或 300mg 的 ARO-ANG3(Q3M)。
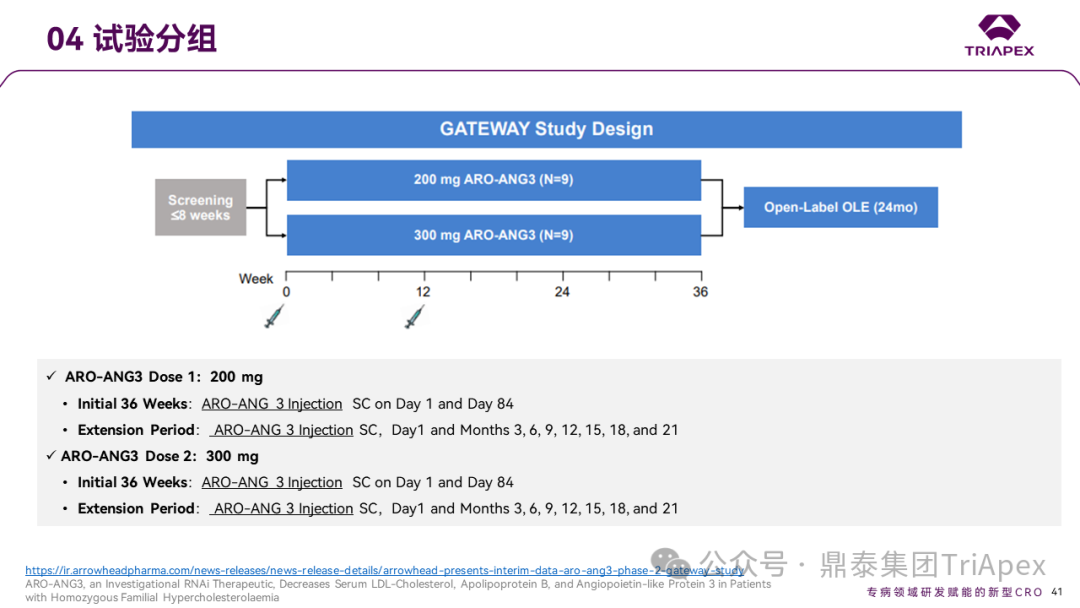
Ⅱ 期临床GATEWAY试验分组[9,10]
主要终点是空腹 LDL-C 从基线到第 24 周的百分比变化。次要终点包括每次评估(空腹)时 LDL-C、ANGPTL3、总 ApoB、HDL-C、TG 和 Non-HDL-C 相对基线的百分比和绝对变化。
第 20 周时,200mg、300mg 剂量组 LDL-C(Martin-Hopkins)分别降低 4.4、 5.0 mmol/L和48.1%、44.0%;ApoB分别降低0.97、0.89 g/L 和 39.2%、34.5%;ANGPTL3 分别降低 82.7%、80.1%。ARO-ANG3 对 ANPTL3 的抑制也降低了 HDL-C、non-HDL-C 和 TG。
HoFH 患者中没有新发现的 AE;没有导致停药、剂量中断或研究退出的 TEAE;在具有广泛动脉粥样硬化性心血管疾病史的患者中报告了一例二级房室传导阻滞的严重不良事件,被认为与 ARO-ANG3 无关。
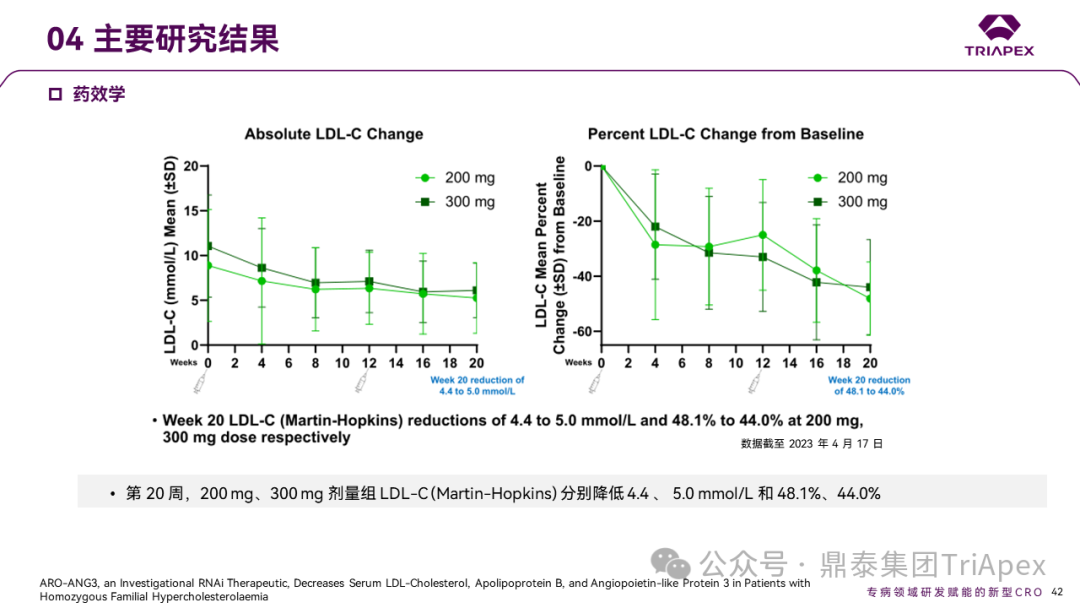
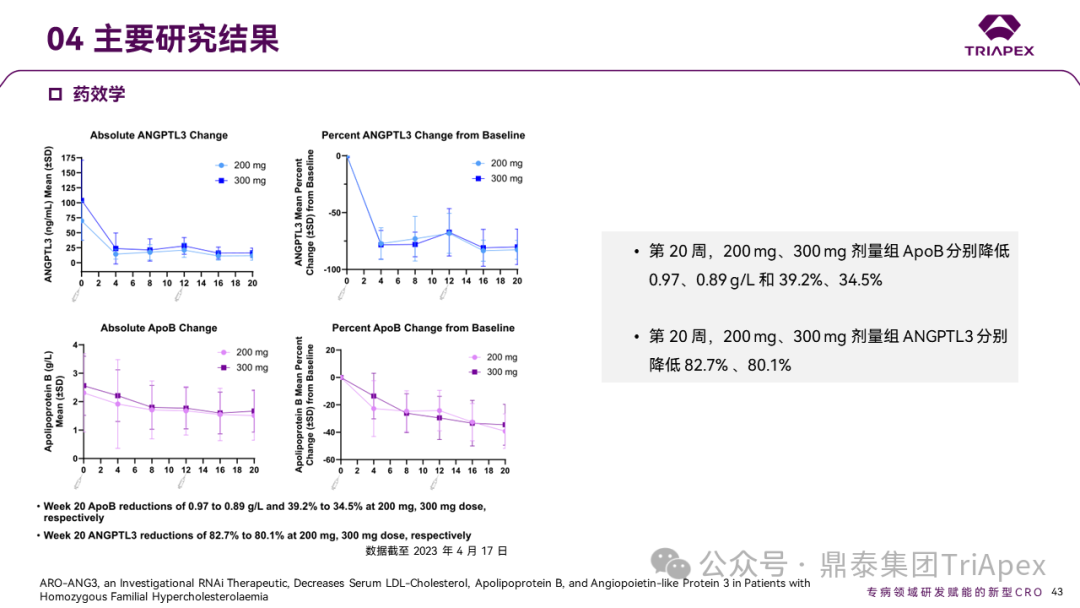
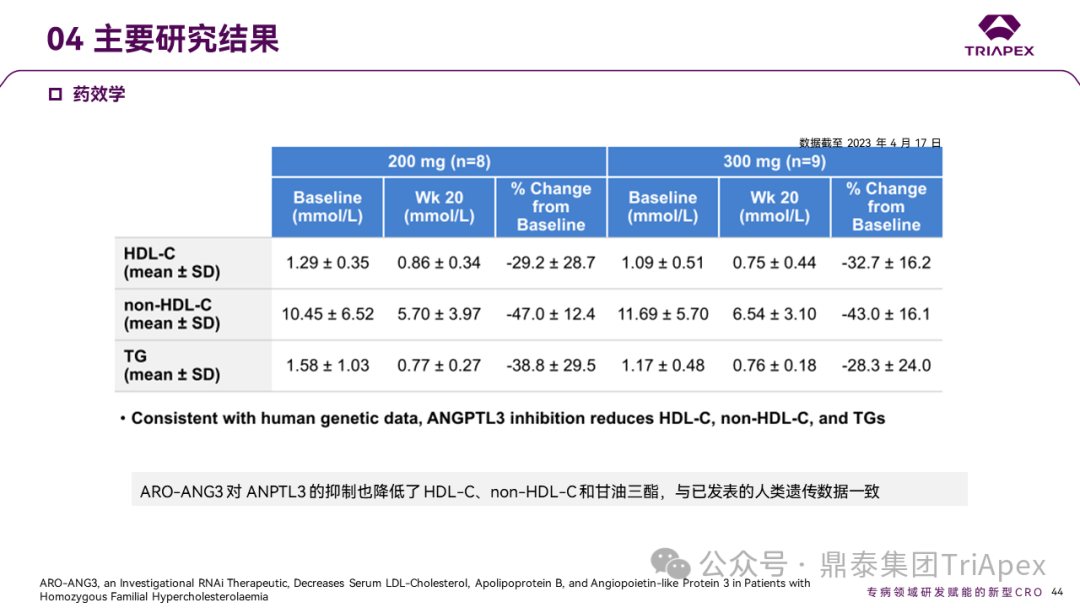
Ⅱ期临床GATEWAY主要研究结果
这些中期数据提示,接受标准降脂治疗的 HoFH 患者接受 ARO-ANG3 治疗后,LDL-C 水平进一步降低,与 ANGPTL3 单抗相似,支持 ARO-ANG3 在 HoFH 患者中的进一步研究[10]。
展望
ANGPTL3 在脂代谢中起着重要作用,抑制 ANGPTL3 可以有效增强 LPL 和 EL 活性,调节富含 TG 的脂蛋白和脂质代谢,并降低心血管事件的风险。除了降低 TG 外,ANGPTL3 还能调控血浆 LDL-C 和 TG 水平。他汀类药物和 PCSK9 单抗等传统降脂疗法依赖于 LDL 受体表达。ANGPTL3 的降胆固醇作用引起了人们对 ANGPTL3 作为治疗对传统疗法反应不佳或不表达功能性 LDLR 的高胆固醇血症患者的靶点的兴趣。
目前,ANGPTL3 靶点还没有 siRNA 产品上市。ANGPTL3 在血脂异常和代谢疾病的研究中越来越受到关注。随着临床试验的不断推进,ANGPTL3 siRNA 治疗的安全性和有效性逐渐得到验证。这一领域的发展将极大推动血脂异常及相关代谢疾病的治疗进程。我们会持续关注这一领域的最新研究进展,以便为药物的开发提供有利支持。
鼎泰团队在 siRNA 药物的非临床药效学、药代动力学、毒理学研究、注册申报和临床开发方面积累了丰富的行业经验。目前,我们已完成多个ANGPTL3 siRNA 相关研究,积累了大量与疾病动物模型、药效学和毒理学数据解读相关的经验。此外,我们对差异化临床试验的开展也有独到的见解。这些综合经验的积累将有助于推动更多差异化 ANGPTL3 siRNA 药物的临床开发和上市进程。

NHP 肥胖模型,来源:鼎泰集团内部数据
在以往的 siRNA 药物研发路径和临床开发历程中,我们深刻认识到,非临床研究不仅为临床试验设计提供了基础数据,还为药物的安全性和有效性评估提供了保障。通过对动物模型的深入研究,我们能够更好地理解药物的作用机制和潜在风险,从而为临床试验的成功奠定基础。
鼎泰团队将继续致力于推动 siRNA 药物的研发,利用我们在非临床研究中的丰富经验,助力 ANGPTL3 siRNA 药物在临床开发中的成功应用。我们相信,这些努力将为患者带来更有效的治疗选择,并推动整个行业的进步。
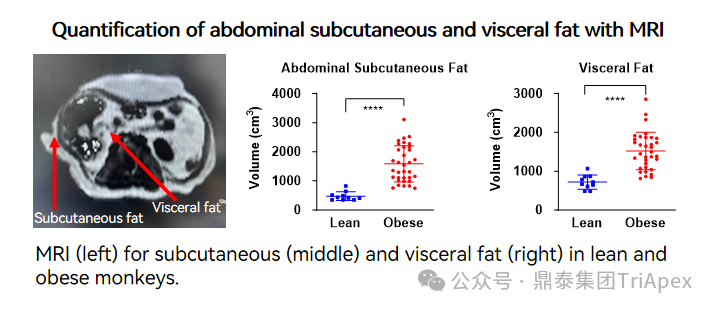
正常动物和肥胖动物腹部皮下脂肪和内脏脂肪含量的对比,来源:鼎泰集团内部数据
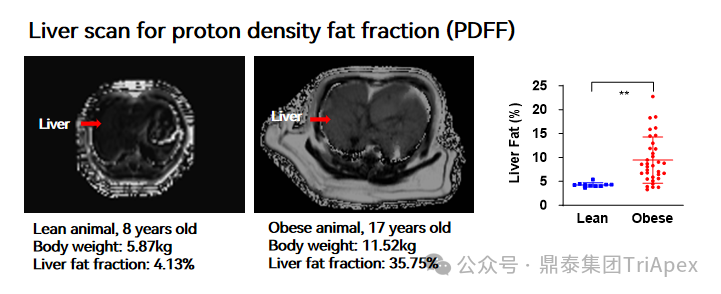
正常动物和肥胖动物肝脏脂肪含量的对比,来源:鼎泰集团内部数据
参考资料:


































































































































