


为推动我国药物安全性评价行业整体能力的提升,中国药学会药物安全评价研究专业委员会于 2024 年 8 月 24-25 日成功主办了 “第七届药物非临床安全性评价专题负责人高级培训班”。大会汇集了 200+位权威专家和资深 SD,共同探讨“ 新产品、新技术、新形势下的药物非临床安全性评价”。
会议厅外,鼎泰集团展台人潮涌动,热闹非凡。会议厅内,鼎泰智慧与行业同仁交融碰撞,共探赋能之路。鼎泰团队分享的《毒理学研究结果与首次人体试验(FIH)起始剂量设计、剂量优化》主题的报告现场互动积极,反响热烈,在此整理分享,望能以飨同道,共享参考。
全文共:1940字 51 图
预计阅读时长:20分钟
毒理学研究结果与首次人体试验(FIH)
起始剂量设计、剂量优化
报告首先从非临床毒理学研究在“双向转化”中发挥的重要作用开始,引出本次分享的主旨内容 —— 毒理学研究结果与 FIH 起始剂量及其在临床剂量优化中的作用。
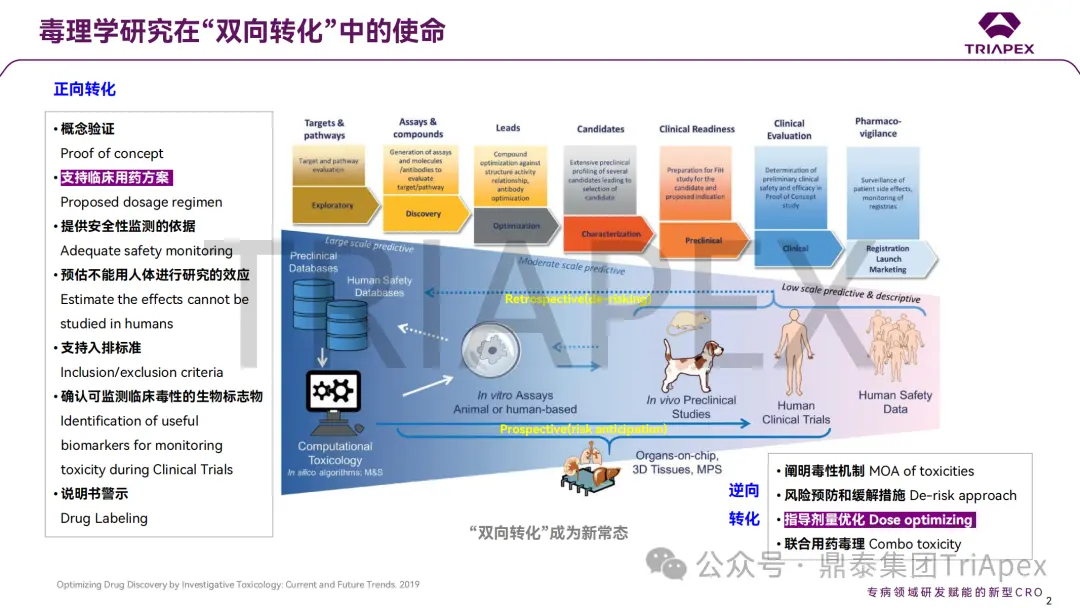
■ 第一部分 FIH 起始剂量设计和剂量递增的指导原则
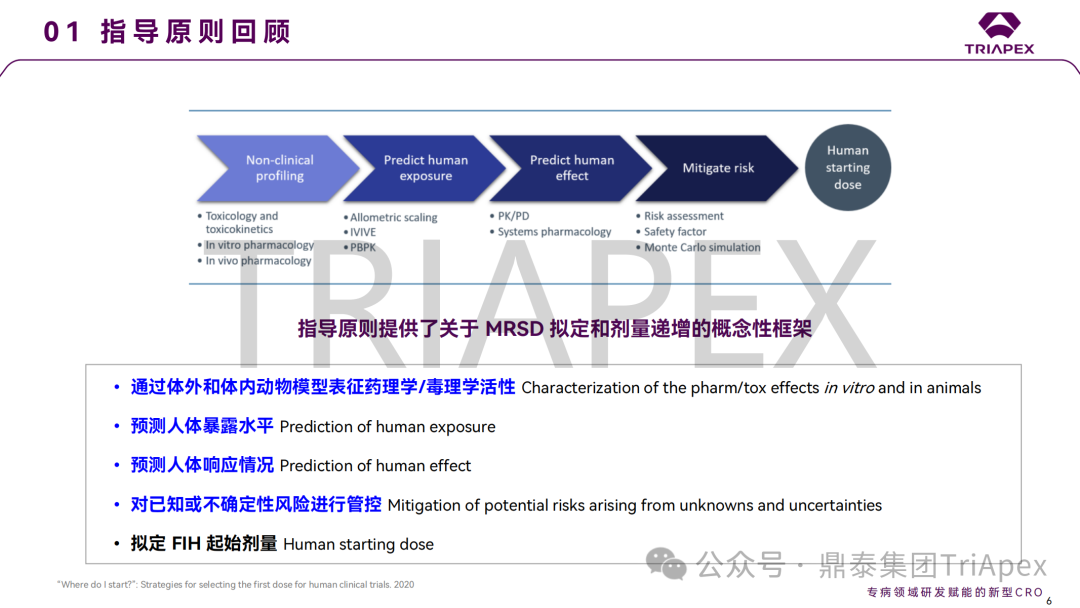
本部分系统回顾了 FDA、EMA、NMPA 等监管机构指导原则和 ICH S9 中与 FIH 起始剂量设计、剂量递增间隔和最大递增剂量相关的建议,包括最大推荐起始剂量(MRSD)的拟定、安全系数的选择等。分析了这些指导原则在不同受试者群体(健康志愿者、晚期肿瘤患者)和不同药物类型(小分子化学药物、ADC、基因重组生物技术药物等)中的适用场景,这些指导原则为 FIH 起始剂量的拟定提供了概念性框架。
此外,在本部分的最后,我们也认识到随着产品类型不断迭代、FIH 方案不断创新,需在参考指导原则的同时,基于对产品特点的理解,综合毒理学、PK、PD 结果具体分析。


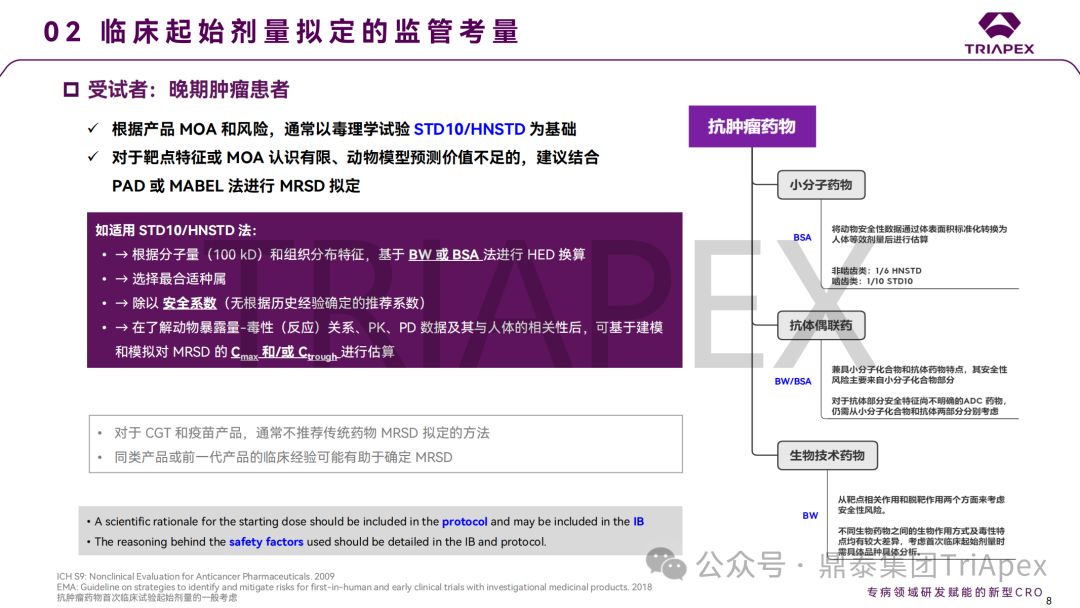



■ 第二部分 工业界的经验与教训
根据第一部分所述指导原则,以晚期肿瘤患者和健康志愿者为受试者的 FIH 试验在安全性和有效性关注程度上有所不同。本部分分别以 11 个已上市 ADC 药物和 6 个已上市 siRNA 药物为例,总结了不同场景下 FIH 起始剂量拟定和剂量递增时的主要考量依据。这些案例构成了当前工业界对于不同场景下起始剂量设计和确定剂量递增间隔的常规经验。
然而,仅仅遵循指导原则而开展非临床研究和进行起始剂量拟定并不总是安全范式。在本部分还借助 TGN1412(2006年)和 BIA-10-2474(2016年)FIH 试验过程中发生的重大医学事件,分享了因起始剂量和剂量递增方案设计不当所带来的经验教训。这些惨痛的案例发人深省,尽管已经过去了 10~20 年的时间,但其教训仍然历历在目、发人深省。
■ 第三部分 毒理学研究结果如何支持临床给药方案
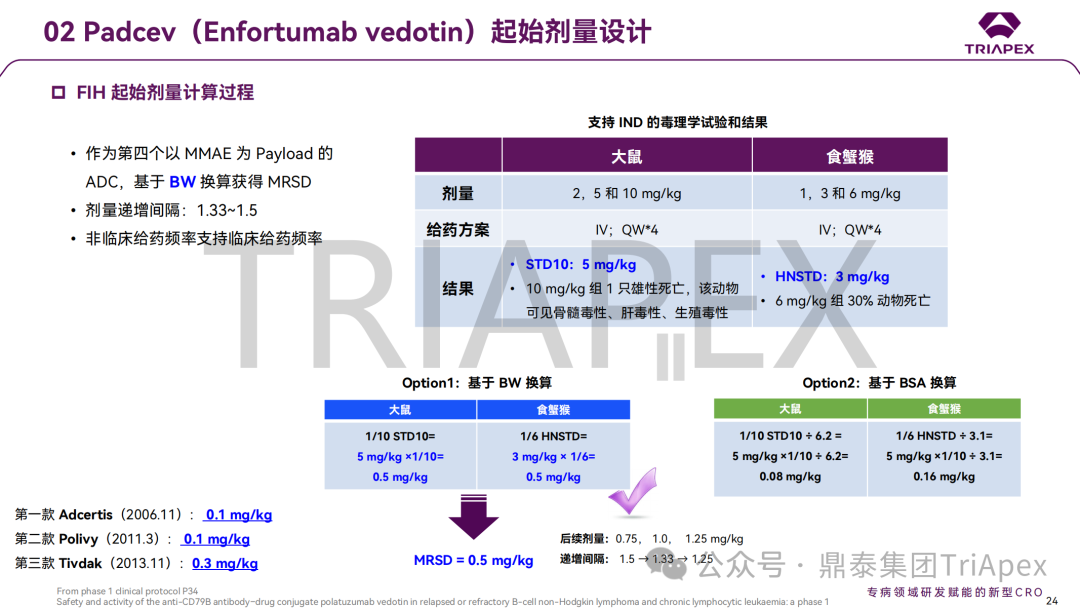
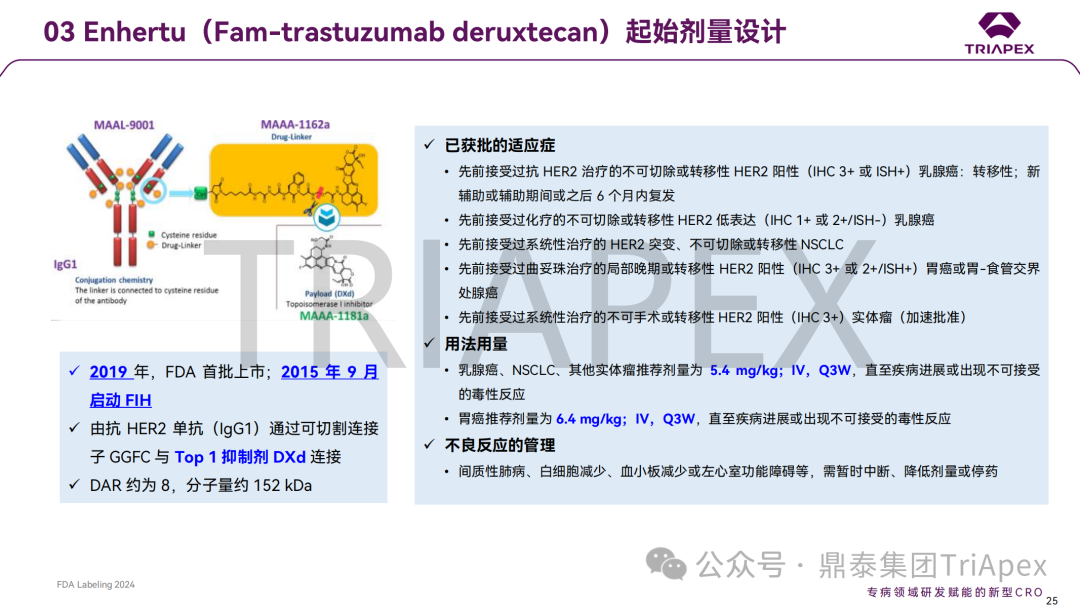
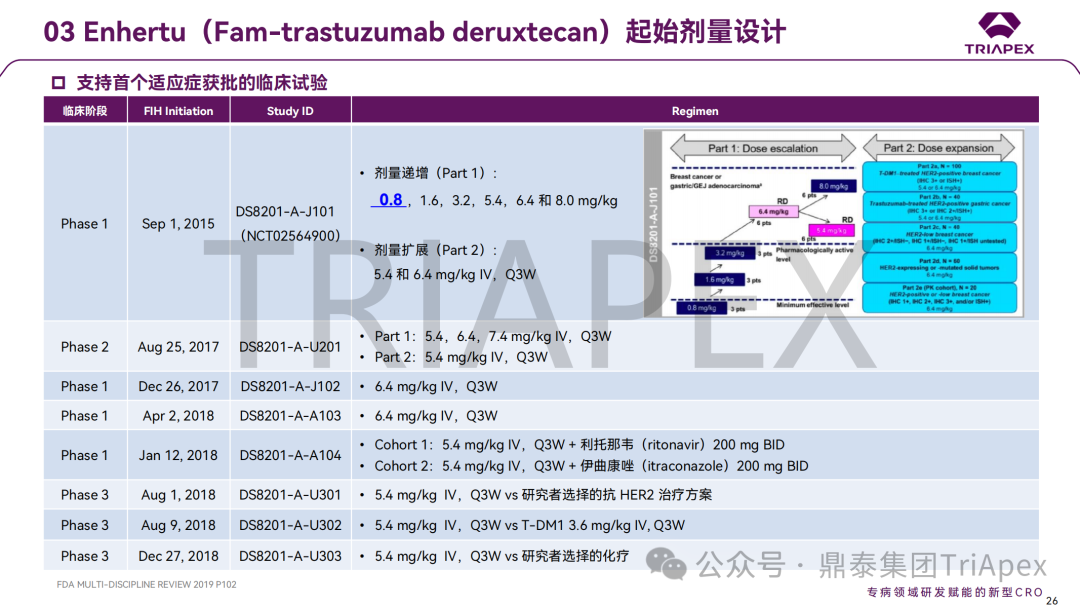
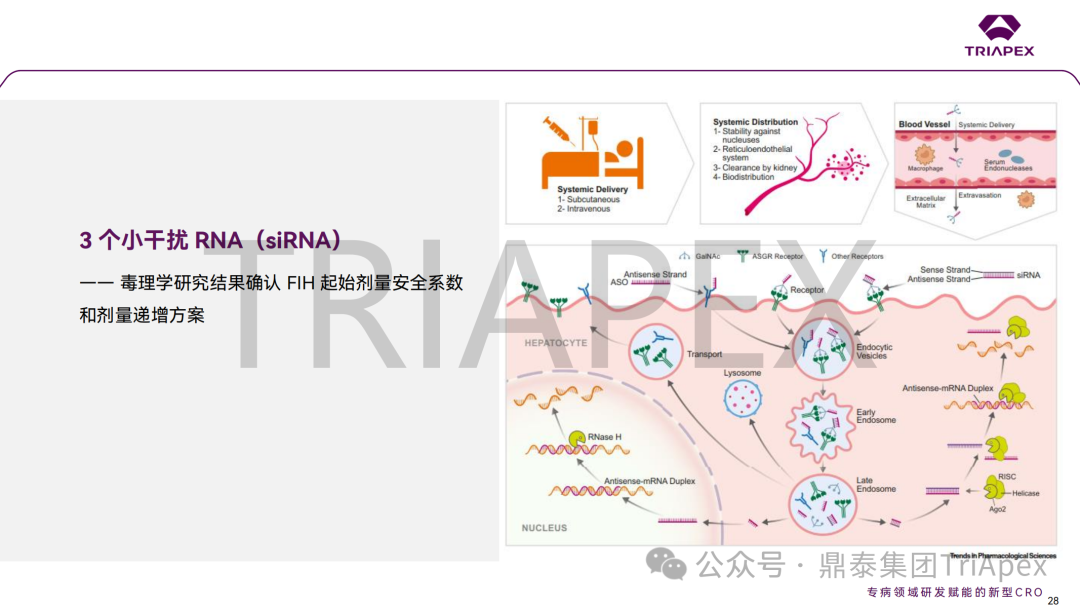
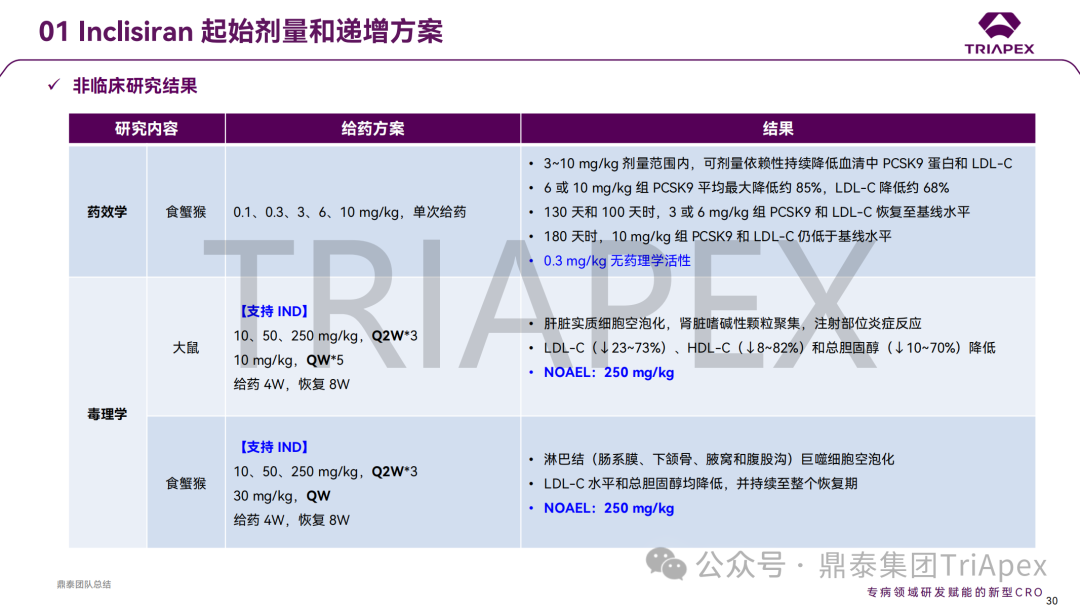
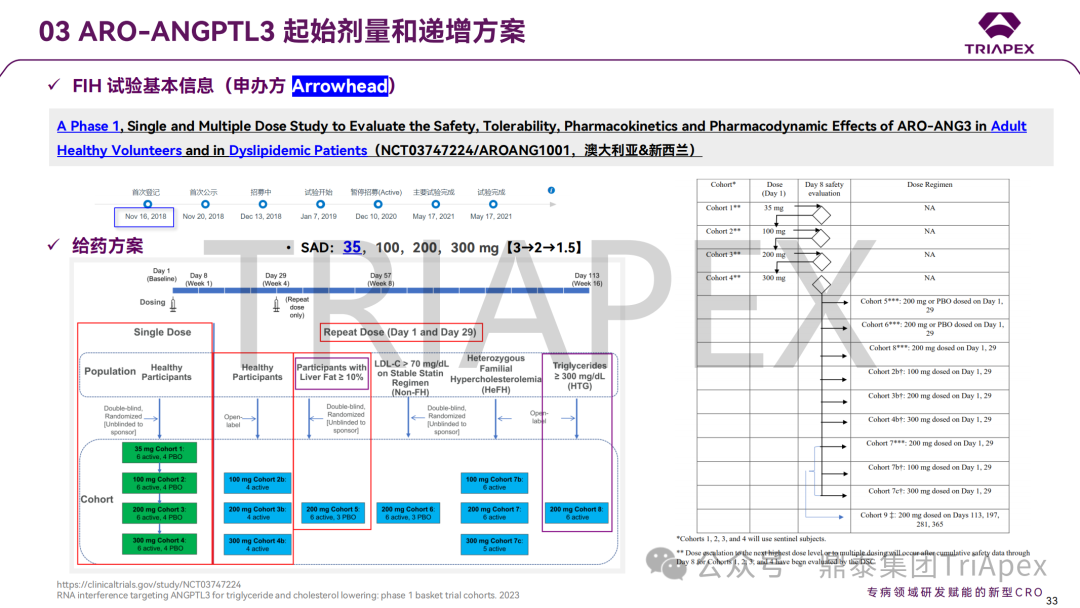
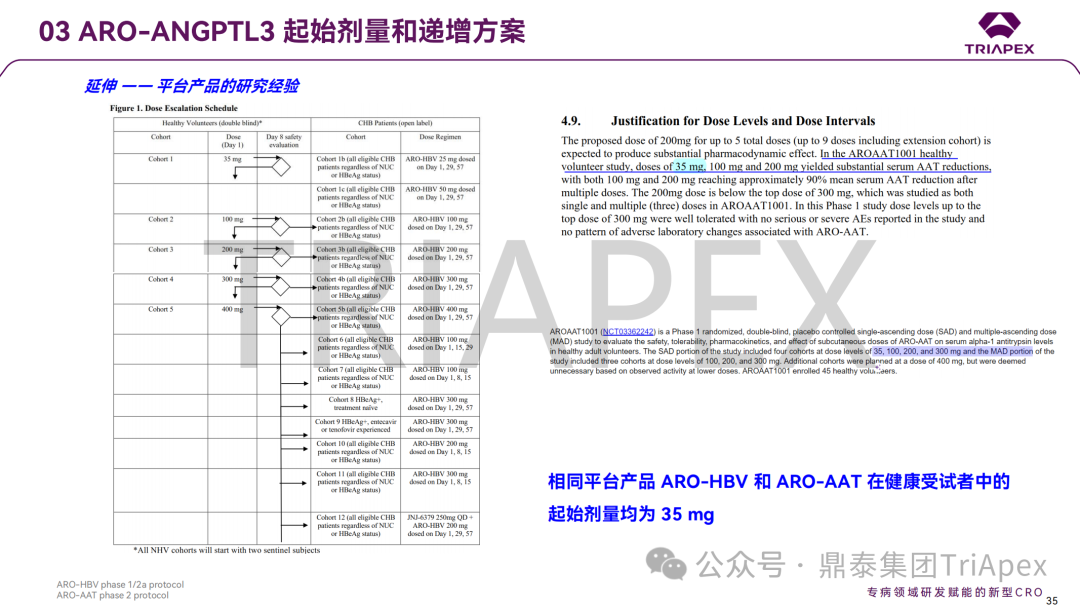
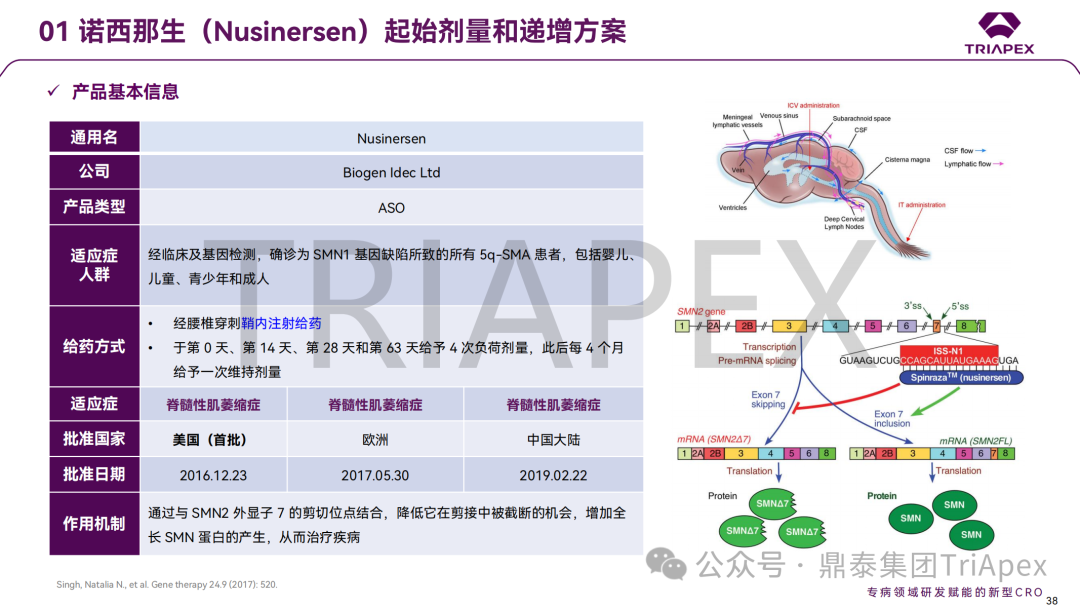
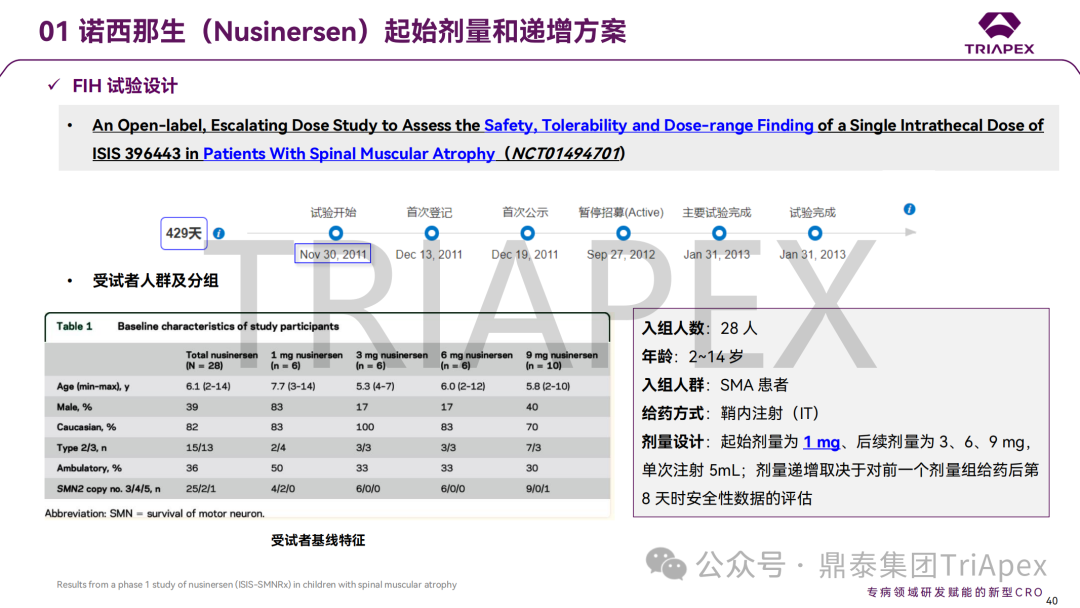
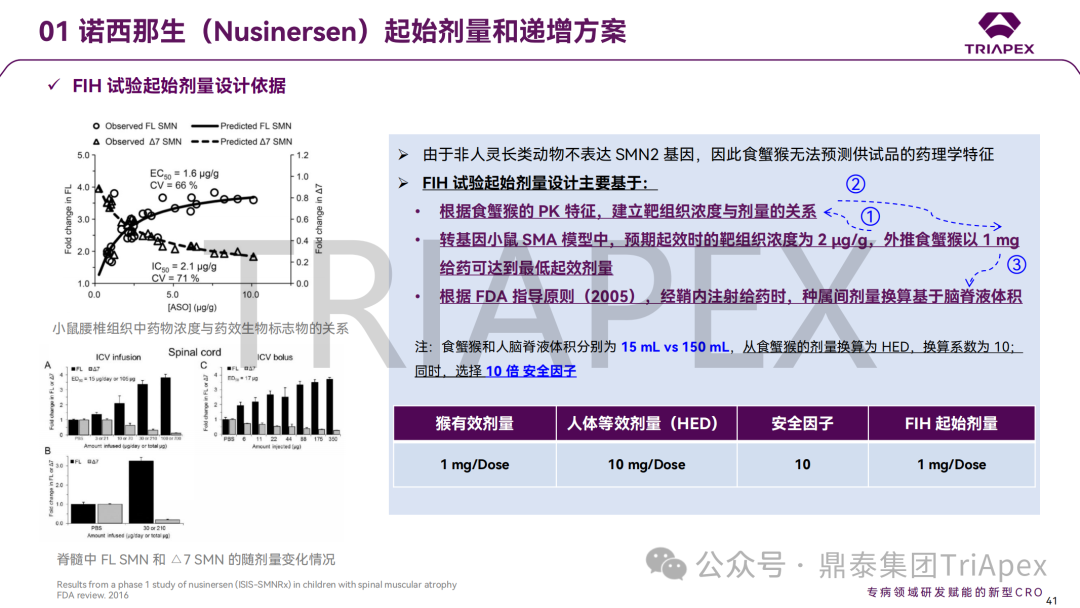
通过三个大类共 8 个案例(其中 3 个 ADC 药物、3 个 siRNA 药物、1 个鞘内注射给药的 ASO 和 1 个玻璃体腔注射给药的双特异性抗体)分析了起始剂量拟定的详细过程,深入探讨不同药物类型和临床试验场景下,毒理学研究结果在起始剂量拟定及指导剂量优化过程中的价值;并分享了单纯依靠毒理学数据进行上述转化研究时面临的局限性。
这些案例汇总了当前主流产品如何通过非临床研究支持临床开发的实操经验,为指导当前研发热点(如 ADC、siRNA 和局部用药的基因治疗产品)提供了有价值的参考。














■ 第四部分 鼎泰的理解与实践
作为一家在专病领域研发赋能的新型 CRO,鼎泰集团始终致力于为全球医药企业和科研机构的新药研发提供高转化价值的服务。在本部分,分享了鼎泰集团在如何通过前瞻性的试验设计和基于对临床研究需求的理解更为精准地进行非临床研究的思考与实践,也分享了鼎泰团队在传统评价手段的基础上,对于新技术领域的积极探索,如基于能更好地模拟患者基因型和疾病表型的 NHP 模型、转基因动物模型、基于器官芯片的体外毒性评估等,以期更好地预测供试品在人体的暴露情况和响应情况。
此外,鼎泰集团还注重整合多学科的专业力量,建立了由毒理学家、药代动力学家、药效学家等组成的跨功能团队。通过内部的学术交流和外部的学术合作,不断提升自身的专业水平和前瞻性思维。







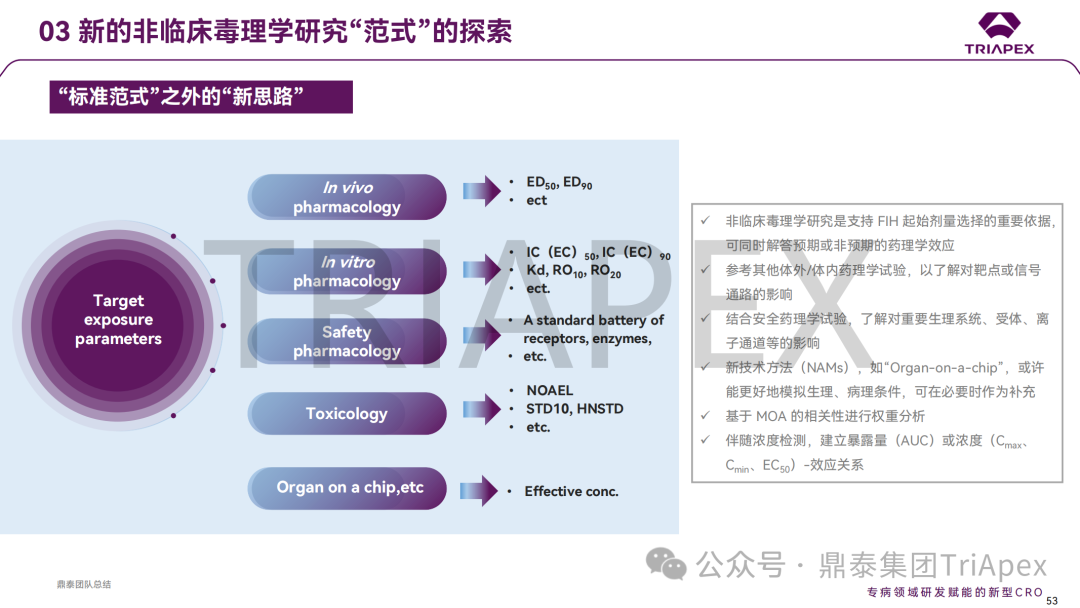
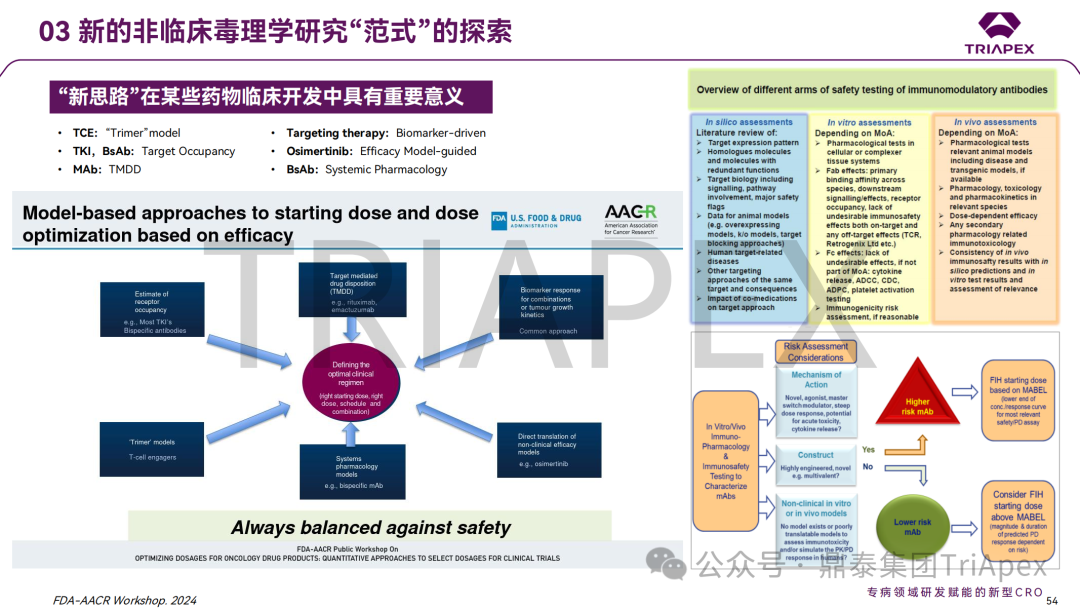
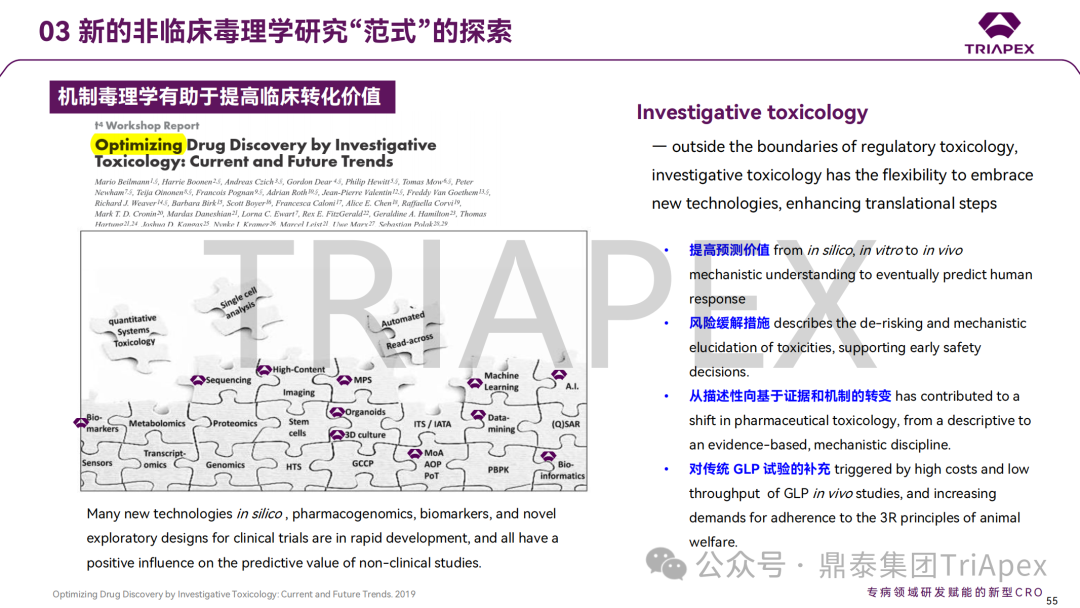
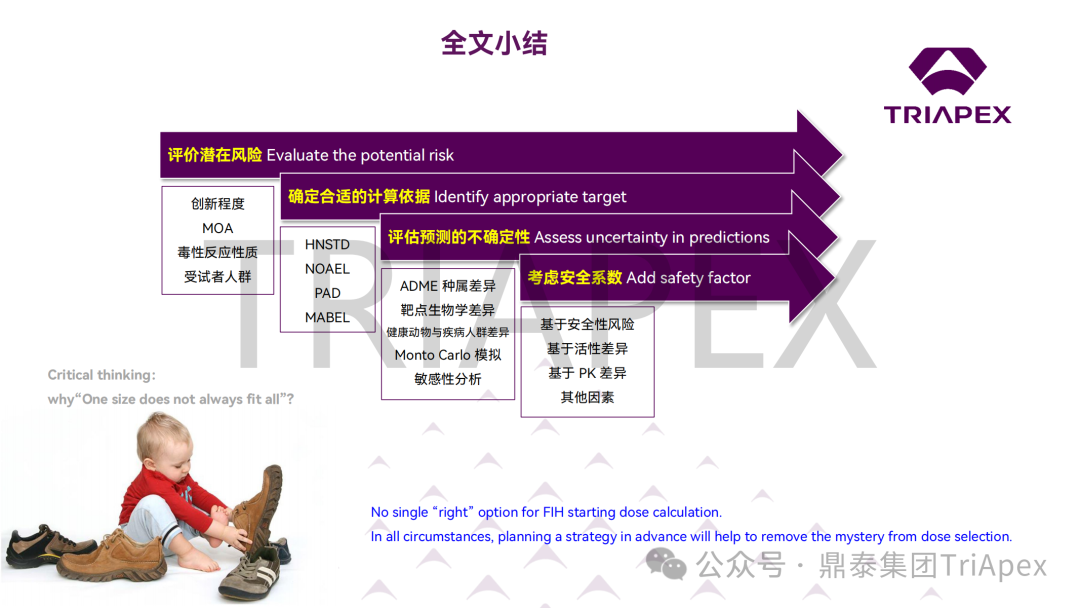

综上,本次报告系统梳理了 FIH 起始剂量设计和剂量递增的相关指导原则,进一步结合工业界的经验和教训,探讨了毒理学研究在临床转化中的价值和不足。更为重要的是,鼎泰团队也分享了自身在这一领域的理解和实践,有望为与会者和行业同仁提供宝贵的见解。
在未来,鼎泰集团将继续深耕毒理学研究在临床转化中的应用,致力于为客户提供更加精准、高效的非临床研究支持。团队将持续关注行业前沿技术的发展,积极探索更具有临床转化价值的非临床研究新思路,为新药研发贡献鼎泰智慧。


































































































































