


关于BA1202及其作用机制
BA1202是国内首个进入临床阶段的CEA/CD3双特异性抗体,拟用于实体瘤的治疗,包括结直肠癌、非小细胞肺癌、胰腺癌和胃癌等CEA阳性肿瘤。
根据博安生物新闻稿,BA1202是靶向CD3和CEA的双特异性抗体,通过同时结合T细胞上的CD3和肿瘤细胞的CEA,将T细胞连接到肿瘤细胞从而杀伤肿瘤细胞。CEACAM5(CEA)在结直肠癌、非小细胞肺癌、胰腺癌和胃癌等上皮性肿瘤细胞的表面广泛表达,而在正常组织中表达较少,是肿瘤靶向治疗的潜在靶点;CD3是T细胞表面的跨膜蛋白,可与T细胞上的TCR结合形成受体复合物激活T细胞,并释放颗粒酶及穿孔素,从而有效杀伤肿瘤细胞。CD3双抗还能增加免疫细胞浸润肿瘤组织,促进“冷肿瘤”转变为“热肿瘤”,提高免疫治疗的敏感性,因而具有与免疫检查点抑制剂联合增效的潜力。因此,BA1202结构和机制新颖,具备单药和联用开发前景。
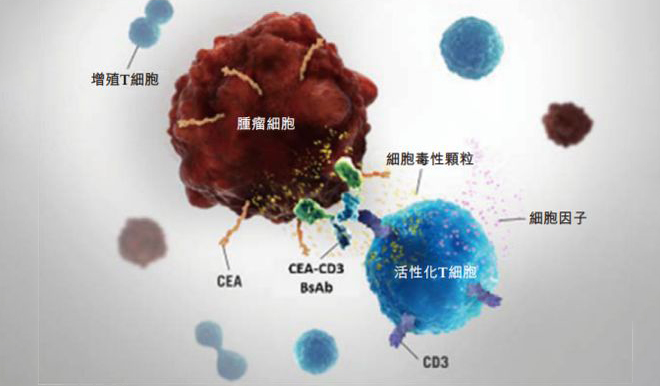
图片来源博安生物官网
关于 BA1202临床试验设计
根据CDE官网公示的临床试验信息,该研究为“一项在晚期实体瘤患者中评价注射用BA1202安全性、耐受性、药代动力学和初步疗效的多中心、开放、单臂、剂量递增和剂量扩展I期临床研究”,主要目的是评价注射用BA1202在晚期实体瘤患者中的安全性和耐受性,观察剂量限制性毒性(DLT),及确定最大耐受剂量(MTD)。研究机构为中国医学科学院肿瘤医院。
根据公示信息,该试验拟采用静脉注射给药。其中,剂量递增阶段共设8个剂量组,每3周给药一次;剂量扩展阶段将根据剂量递增阶段累积的安全性和抗肿瘤疗效等数据,选择1~2个剂量水平进行扩展,每3周给药一次。
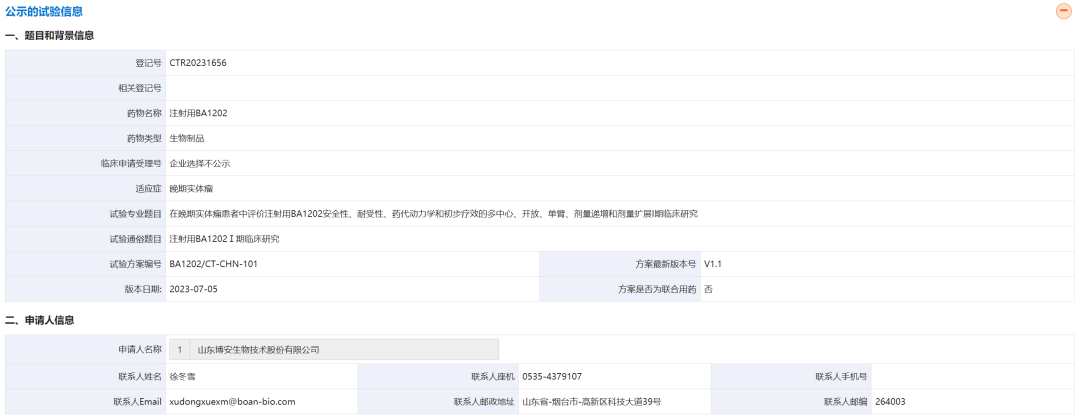
图片来源CDE官网
临床前研究提供了重要的临床转化价值
鼎泰团队有幸参与了BA1202项目的临床前研究,为BA1202的IND申报和临床开发贡献了鼎泰智慧。
BA1202在临床前研究显示出良好的安全性。基于对BA1202产品特点的充分理解和CD3 BiTE非临床研究的丰富经验,鼎泰团队完成了该产品的临床前药代动力学和安全性评价试验,为BA1202提供了合规、高质和高效的服务。以上研究为BA1202的首次人体临床试验方案中关键性设计提供了非临床参考依据,助力该产品完成IND申报并顺利进入临床。
结语
鼎泰团队将继续以专业的技术水平和高效的项目管理体系加快药物创新转化,始终致力于为全球医药企业和科研机构提供一体化的药物研发赋能。
在此,我们衷心地期待BA1202能够通过早期临床试验快速完成临床概念验证(POC),并高效推进至后期临床试验阶段,为结直肠癌、非小细胞肺癌、胰腺癌和胃癌等CEA阳性恶性肿瘤患者提供更为有效的突破性疗法。
关于博安生物


















































































